По своей сути кальцинация — это не одна химическая реакция, а скорее категория процессов, управляемых теплом, определяемых конкретным результатом: термическим разложением. Хотя под этот зонтик подпадают многие реакции, наиболее распространенным примером является распад карбоната, например, нагревание известняка (карбоната кальция) для получения извести (оксида кальция) и углекислого газа.
Кальцинация — это процесс термической обработки, который использует высокую температуру в контролируемой атмосфере для разложения материала. Его основная цель — удалить летучий компонент, такой как углекислый газ или вода, для очистки или изменения химических и физических свойств оставшегося твердого вещества.

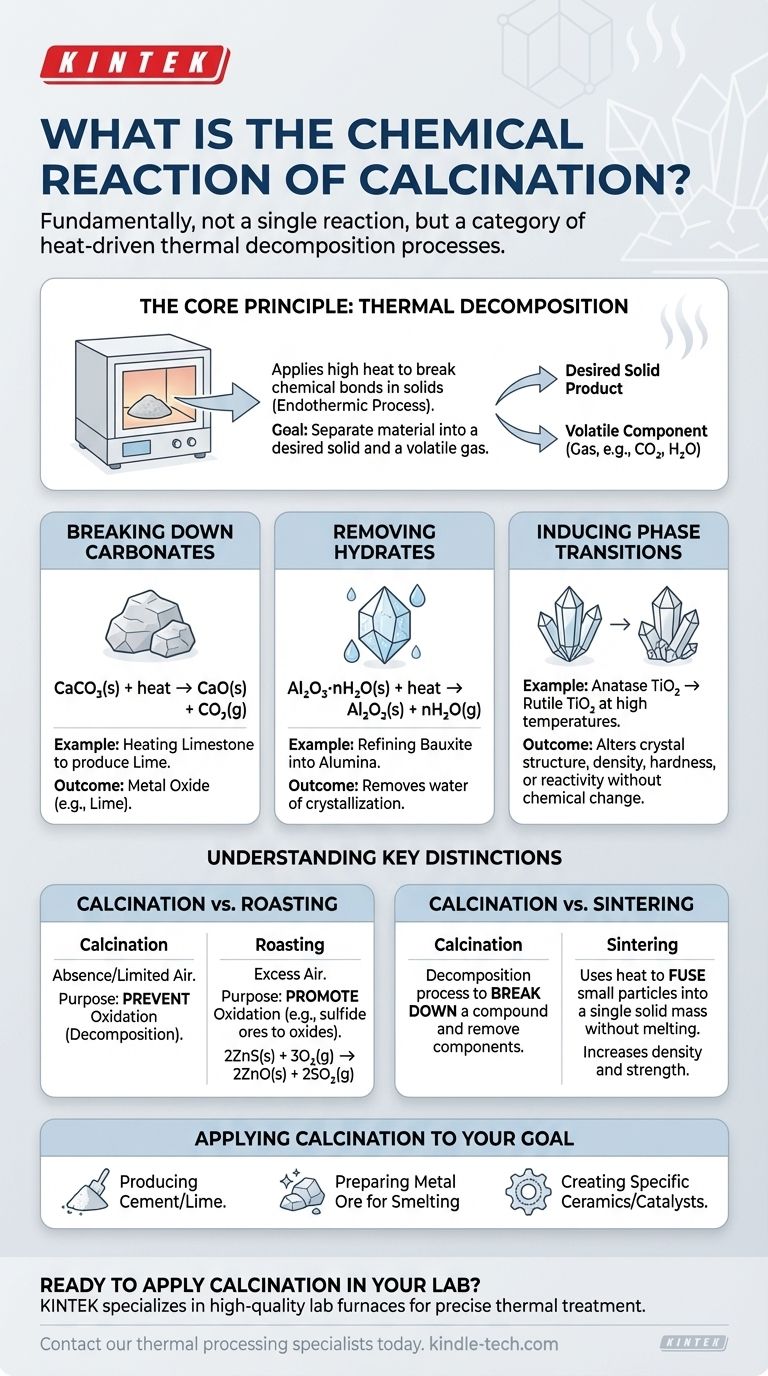
Основной принцип: термическое разложение
Кальцинация работает путем приложения достаточной тепловой энергии к твердому телу для разрыва его химических связей. Этот процесс всегда является эндотермическим, то есть требует затрат энергии (тепла) для протекания. Цель состоит в том, чтобы отделить материал на желаемый твердый продукт и летучий компонент, который может быть удален в виде газа.
Разложение карбонатов
Это классическое и наиболее распространенное применение кальцинации, особенно в производстве цемента. Когда карбонат металла нагревается, он разлагается на оксид металла и углекислый газ.
Для известняка реакция выглядит так:
CaCO₃(s) + heat → CaO(s) + CO₂(g)
Здесь твердый карбонат кальция разлагается на твердый оксид кальция (известь) и газообразный углекислый газ.
Удаление гидратов (кристаллизационной воды)
Многие минералы существуют в виде гидратов, что означает, что молекулы воды включены в их кристаллическую структуру. Кальцинация используется для удаления этой воды, процесс, который часто называют «сушкой», хотя это химическое разложение.
Например, переработка бокситовой руды в глинозем включает кальцинацию гидратированного оксида алюминия:
Al₂O₃·nH₂O(s) + heat → Al₂O₃(s) + nH₂O(g)
Этот этап удаляет воду, концентрируя оксид алюминия, который является необходимым предшественником для производства алюминия.
Индуцирование фазовых переходов
Реже кальцинация может относиться к процессу, при котором тепло не вызывает разложения, а вместо этого изменяет кристаллическую структуру (фазу) материала. Это изменяет его физические свойства, такие как плотность, твердость или реакционная способность, не изменяя его химическую формулу.
Примером является преобразование анатаза, формы диоксида титана (TiO₂), в его более стабильную рутильную фазу при высоких температурах.
Понимание ключевых различий
Ценность кальцинации становится более очевидной при сравнении с другими распространенными термическими процессами. Конкретные условия — особенно атмосфера — определяют результат.
Кальцинация против обжига
Это самое важное различие. Кальцинация происходит в отсутствие или при ограниченном доступе воздуха, чтобы намеренно предотвратить окисление.
Обжиг, напротив, проводится в избытке воздуха специально для содействия окислению. Обычно он используется для сульфидных руд, превращая их в оксиды. Например, обжиг сульфида цинка:
2ZnS(s) + 3O₂(g) → 2ZnO(s) + 2SO₂(g)
Кальцинация против спекания
Эти процессы имеют противоположные цели. Кальцинация — это процесс разложения, используемый для разрушения соединения и удаления компонента.
Спекание же использует тепло (ниже температуры плавления) для сплавления мелких частиц в единую твердую массу. Это увеличивает плотность и прочность, по сути «сваривая» материал вместе, не расплавляя его.
Применение кальцинации к вашей цели
Конкретная реакция кальцинации, которая вас интересует, полностью зависит от вашего исходного материала и желаемого конечного продукта.
- Если ваше основное внимание уделяется производству цемента или извести: вы используете кальцинацию для разложения карбоната кальция в реакционноспособный оксид кальция.
- Если ваше основное внимание уделяется подготовке металлической руды к плавке: вы, вероятно, используете кальцинацию для удаления воды (из гидратов) или углекислого газа (из карбонатов) для обогащения содержания металла.
- Если ваше основное внимание уделяется созданию определенной керамики или катализатора: вы можете использовать кальцинацию для достижения желаемой кристаллической фазы и удельной поверхности в таких материалах, как глинозем или титания.
В конечном счете, кальцинация является основополагающим инструментом в материаловедении для преобразования сыпучих твердых веществ в более полезные, концентрированные или реакционноспособные формы.
Сводная таблица:
| Тип реакции кальцинации | Пример реакции | Ключевой результат |
|---|---|---|
| Разложение карбоната | CaCO₃(s) + heat → CaO(s) + CO₂(g) |
Образует оксид металла (например, известь) |
| Разложение гидрата | Al₂O₃·nH₂O(s) + heat → Al₂O₃(s) + nH₂O(g) |
Удаляет кристаллизационную воду |
| Фазовый переход | Анатаз TiO₂ → Рутил TiO₂ | Изменяет кристаллическую структуру и свойства |
Готовы применить кальцинацию в своей лаборатории?
Независимо от того, разрабатываете ли вы новые катализаторы, перерабатываете руды или синтезируете передовую керамику, точная термическая обработка имеет решающее значение. KINTEK специализируется на высококачественных лабораторных печах и оборудовании, предназначенном для надежных процессов кальцинации.
Мы предоставляем инструменты, необходимые для достижения равномерного нагрева, точного контроля температуры и стабильных результатов. Позвольте нашим экспертам помочь вам выбрать правильное оборудование для вашего конкретного материала и применения.
Свяжитесь с нашими специалистами по термической обработке сегодня, чтобы обсудить требования вашего проекта и узнать, как KINTEK может улучшить ваши исследования и разработки.
Визуальное руководство
Связанные товары
- Электрическая вращающаяся печь для пиролиза, установка, машина, кальцинатор, малая вращающаяся печь, вращающаяся печь
- Электрическая вращающаяся печь непрерывного действия, малая вращающаяся печь, установка для пиролиза с нагревом
- Вертикальная высокотемпературная вакуумная графитизационная печь
- Графитовая вакуумная печь для графитации пленки с высокой теплопроводностью
- Графитировочная печь сверхвысоких температур в вакууме
Люди также спрашивают
- Каковы характеристики режимов движения слоя скольжения, обрушения и перекатывания? Оптимизируйте ваш роторный процесс
- При какой температуре происходит пиролиз? Руководство по контролю выхода вашей продукции
- Какова температура вращающейся печи? Это зависит от вашего материала и цели процесса
- Какие бывают типы кальцинаторов? Руководство по выбору подходящего оборудования для термической обработки
- Каковы принципы работы вращающейся печи? Освойте механику высокотемпературной обработки



















