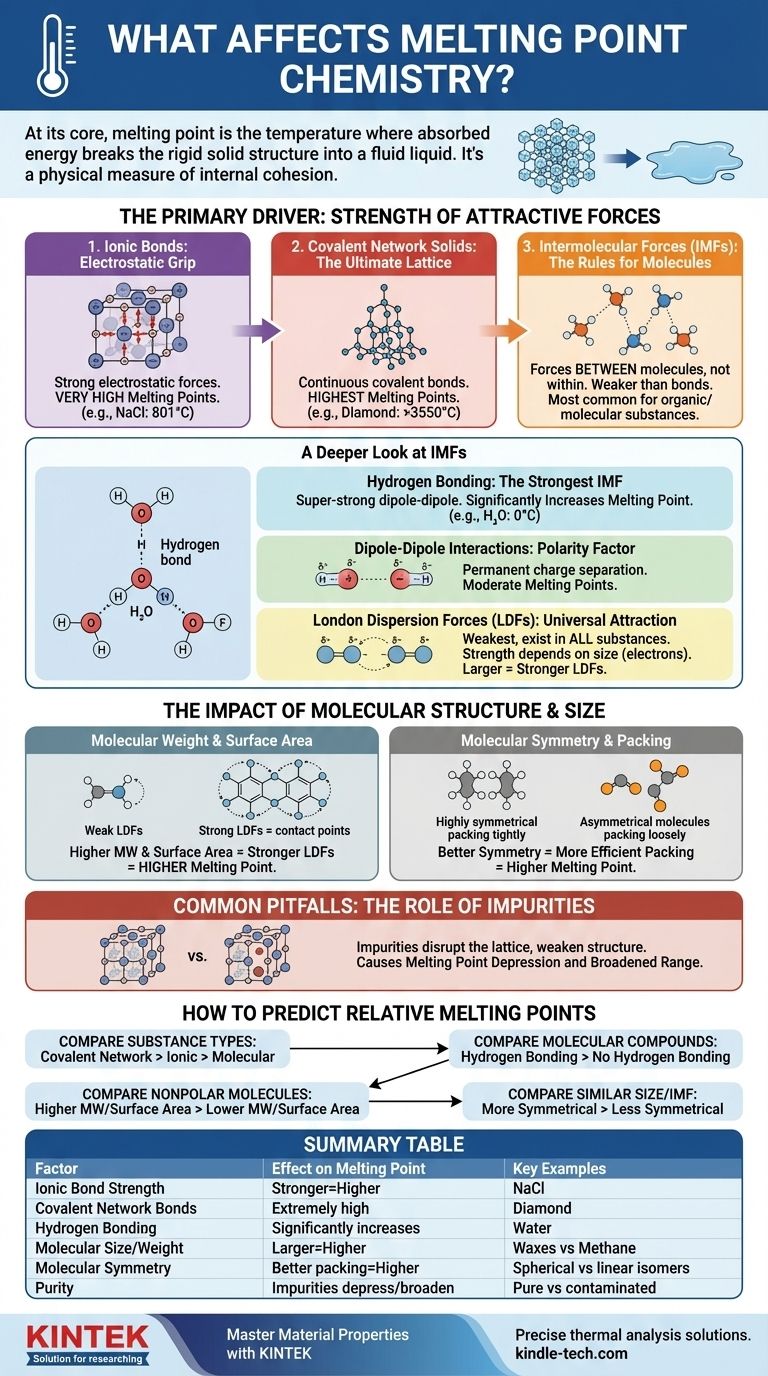
По своей сути, температура плавления вещества — это температура, при которой оно поглотило достаточно энергии, чтобы разрушить жесткую, упорядоченную структуру твердого тела и перейти в неупорядоченное, текучее жидкое состояние. Это определяется двумя основными факторами: силой притяжения, удерживающей частицы (атомы, ионы или молекулы) вместе, и эффективностью, с которой эти частицы упаковываются в твердую кристаллическую решетку.
Температура плавления — это не просто число; это физическая мера внутренней когезии вещества. Чтобы понять ее, вы должны сначала определить доминирующую силу, удерживающую частицы вместе — будь то мощная ионная связь или слабое межмолекулярное притяжение — а затем рассмотреть, как размер и форма молекул уточняют это значение.

Основной фактор: сила притяжения
Количество энергии, необходимое для разрушения твердой решетки, прямо пропорционально силе удерживающих ее сил. Эти силы существуют в широком спектре, от невероятно сильных химических связей до гораздо более слабых межмолекулярных сил.
Ионные связи: электростатическое сцепление
Ионные соединения, такие как поваренная соль (NaCl), удерживаются вместе мощными электростатическими притяжениями между положительными и отрицательными ионами. Эти силы создают очень стабильную кристаллическую решетку.
Преодоление этих сильных притяжений требует огромного количества тепловой энергии, поэтому ионные соединения обычно имеют очень высокие температуры плавления.
Ковалентные сетчатые твердые тела: идеальная решетка
В ковалентном сетчатом твердом теле, таком как алмаз или кварц (SiO₂), атомы не просто притягиваются друг к другу; они соединены непрерывной сетью сильных ковалентных связей. Нет отдельных молекул для разделения.
Чтобы расплавить такое вещество, вы должны начать разрывать эти мощные ковалентные связи. Это требует больше энергии, чем любой другой тип взаимодействия, что дает этим материалам самые высокие температуры плавления среди всех веществ.
Межмолекулярные силы (ММС): правила для молекул
Для молекулярных соединений (таких как вода, сахар или воск) температура плавления связана не с разрывом ковалентных связей внутри молекул. Она связана с преодолением более слабых сил притяжения между молекулами. Они известны как межмолекулярные силы (ММС).
Более глубокий взгляд на межмолекулярные силы (ММС)
Тип и сила ММС являются единственным наиболее важным фактором для определения температуры плавления большинства органических и молекулярных веществ. Они, как правило, намного слабее полноценных химических связей.
Водородная связь: сильнейшая ММС
Это особый, сверхсильный тип диполь-дипольного взаимодействия, который возникает, когда водород связан с сильно электроотрицательным атомом, таким как азот (N), кислород (O) или фтор (F).
Возникающее притяжение между молекулами значительно. Вода (H₂O) является классическим примером; ее водородные связи дают ей гораздо более высокую температуру плавления (0 °C), чем можно было бы ожидать для молекулы такого размера.
Диполь-дипольные взаимодействия: фактор полярности
Полярные молекулы имеют постоянное разделение заряда, создавая положительный и отрицательный конец, как крошечные магниты. Эти молекулярные «полюса» притягиваются друг к другу.
Эти силы сильнее, чем силы между неполярными молекулами аналогичного размера, что приводит к умеренным температурам плавления.
Лондоновские дисперсионные силы (ЛДФ): универсальное притяжение
ЛДФ — это самый слабый тип ММС, и они существуют во всех веществах. Они возникают из случайных, временных флуктуаций в распределении электронов вокруг молекулы, что создает мимолетные, мгновенные диполи.
Сила ЛДФ напрямую зависит от размера молекулы (в частности, от количества ее электронов). Более крупные молекулы имеют более крупные, более «рыхлые» электронные облака, что делает их более поляризуемыми и приводит к более сильным ЛДФ. Вот почему крупные неполярные молекулы, такие как воск, могут оставаться твердыми при комнатной температуре.
Влияние молекулярной структуры и размера
Помимо типа силы, специфическая форма и размер молекулы играют решающую роль в уточнении ее температуры плавления.
Молекулярный вес и площадь поверхности
Для молекул с одинаковой доминирующей ММС (например, при сравнении двух неполярных молекул) та, которая имеет более высокий молекулярный вес, будет иметь более сильные ЛДФ и, следовательно, более высокую температуру плавления. Большая площадь поверхности позволяет большему количеству точек контакта между молекулами, что также усиливает ЛДФ.
Молекулярная симметрия и упаковка
Симметрия оказывает глубокое влияние. Высокосимметричные молекулы могут более эффективно и плотно упаковываться в стабильную кристаллическую решетку, как хорошо сделанные кирпичики LEGO.
Это плотное, упорядоченное расположение требует больше энергии для разрушения. Поэтому более симметричная молекула часто будет иметь значительно более высокую температуру плавления, чем менее симметричный изомер, даже если они имеют одинаковую формулу и вес.
Распространенные ошибки, которых следует избегать: роль примесей
В практическом, реальном контексте одним из наиболее распространенных факторов, влияющих на температуру плавления, является чистота образца.
Нарушение кристаллической решетки
Примеси — это посторонние частицы, которые не вписываются аккуратно в кристаллическую решетку вещества. Они вызывают дефекты и ослабляют общую структуру.
Поскольку решетка уже нарушена, для ее разрушения требуется меньше энергии, что приводит к более низкой температуре плавления. Это явление известно как депрессия температуры плавления.
Расширенный диапазон плавления
Чистое вещество обычно плавится в очень узком температурном диапазоне (часто менее 1 °C). Присутствие примесей не только снижает температуру плавления, но и приводит к тому, что вещество плавится в более широком, расширенном температурном диапазоне. Химики используют эту характеристику для оценки чистоты синтезированного соединения.
Как предсказать относительные температуры плавления
При сравнении двух веществ пройдите по этой иерархии вопросов, чтобы сделать точный прогноз.
- Если ваша основная цель — сравнение различных типов веществ: Ковалентное сетчатое твердое тело (алмаз) будет иметь более высокую температуру плавления, чем ионное соединение (соль), которая будет намного выше, чем у молекулярного соединения (сахар).
- Если ваша основная цель — сравнение двух молекулярных соединений: Сначала проверьте наличие водородных связей. Молекула, которая может образовывать водородные связи, почти всегда будет иметь более высокую температуру плавления, чем та, которая не может, при условии аналогичного размера.
- Если ваша основная цель — сравнение двух неполярных молекул: Молекула с более высоким молекулярным весом и большей площадью поверхности будет иметь более сильные лондоновские дисперсионные силы и более высокую температуру плавления.
- Если ваша основная цель — сравнение двух молекул аналогичного размера и типа ММС: Более симметричная молекула, которая может более эффективно упаковываться в кристаллическую решетку, вероятно, будет иметь более высокую температуру плавления.
Понимание этих факторов превращает температуру плавления из простого значения данных в мощный индикатор фундаментальных молекулярных сил и структуры вещества.
Сводная таблица:
| Фактор | Влияние на температуру плавления | Ключевые примеры |
|---|---|---|
| Сила ионной связи | Более сильные связи = Более высокая температура плавления | Хлорид натрия (NaCl): 801°C |
| Ковалентные сетчатые связи | Чрезвычайно высокие температуры плавления | Алмаз: >3550°C |
| Водородная связь | Значительно увеличивает температуру плавления | Вода (H₂O): 0°C |
| Молекулярный размер/вес | Более крупные молекулы = Более высокая температура плавления (более сильные ЛДФ) | Воски (высокий ММ) против метана (низкий ММ) |
| Молекулярная симметрия | Лучшая упаковка = Более высокая температура плавления | Сферические против линейных изомеров |
| Чистота | Примеси снижают и расширяют диапазон плавления | Чистые против загрязненных образцов |
Освойте свойства материалов с KINTEK
Понимание температур плавления критически важно для выбора материалов, синтеза и контроля качества в лаборатории. Независимо от того, разрабатываете ли вы новые соединения или анализируете чистоту материалов, наличие правильного оборудования имеет важное значение.
KINTEK специализируется на высококачественном лабораторном оборудовании и расходных материалах, разработанных для обеспечения точного и надежного термического анализа. Наши продукты помогают исследователям и лабораторным специалистам точно определять температуры плавления и понимать поведение материалов.
Готовы расширить возможности вашей лаборатории? Свяжитесь с нашими экспертами сегодня, чтобы найти идеальное решение для ваших потребностей в термическом анализе.
Визуальное руководство