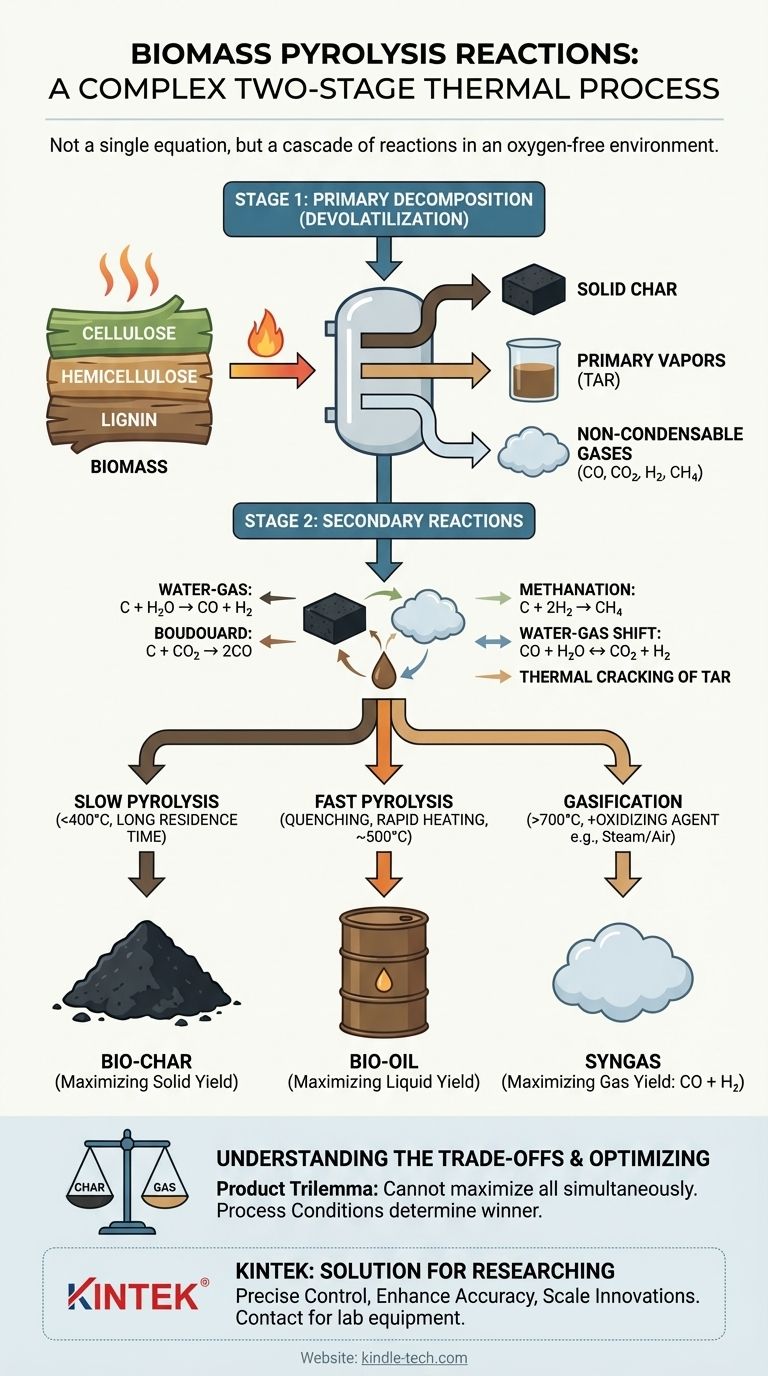
По своей сути, пиролиз биомассы — это не единичная химическая реакция, а сложный двухстадийный термический процесс. Сначала тепло разлагает крупные органические полимеры биомассы в бескислородной среде (процесс, называемый дегазацией), создавая смесь твердого угля, жидких паров (смолы) и газов. Затем эти исходные продукты подвергаются серии вторичных реакций, взаимодействуя друг с другом с образованием конечных стабильных продуктов: биоугля, бионефти и синтез-газа.
Пиролиз лучше всего понимать как каскад реакций, а не как одно уравнение. Начальное термическое крекирование биомассы сопровождается вторичными реакциями с участием образующегося угля и паров. Конечный выход продуктов — угля, масла или газа — полностью определяется тем, какие из этих вторичных путей реакции благоприятствуются условиями процесса, такими как температура и скорость нагрева.

Две стадии реакций пиролиза
Чтобы понять пиролиз, необходимо разделить процесс на две отдельные, но взаимосвязанные стадии. Первая — это начальное разложение твердой биомассы, а вторая — последующее превращение образующихся продуктов.
Стадия 1: Первичное разложение (дегазация)
Это начальное термическое «крекирование» самой биомассы. Тепловая энергия разрывает химические связи внутри основных компонентов биомассы: целлюлозы, гемицеллюлозы и лигнина.
Эта стадия не описывается простым химическим уравнением. Это сложная сеть одновременных реакций разложения, которые превращают твердую биомассу в три основных продукта:
- Твердый уголь: Углеродсодержащий твердый остаток.
- Первичные пары: Конденсирующийся аэрозоль жидкостей, часто называемый смолой или прекурсорами бионефти.
- Неконденсируемые газы: Легкие газы, такие как CO, CO₂, H₂ и CH₄.
Стадия 2: Вторичные реакции
После образования первичных продуктов они продолжают реагировать в горячей среде реактора. Эти вторичные реакции в конечном итоге определяют окончательный состав и выход ваших продуктов. Наиболее важные из них включают реакцию горячего угля с газами и парами, образующимися на Стадии 1.
Ключевые вторичные реакции включают:
- Водяной газ:
C (уголь) + H₂O (пар) → CO + H₂ - Реакция Будуара:
C (уголь) + CO₂ → 2CO - Метанирование:
C (уголь) + 2H₂ → CH₄ - Конверсия водяного газа:
CO + H₂O ↔ CO₂ + H₂
Кроме того, тяжелые смоляные пары могут подвергаться термическому крекингу при высоких температурах, распадаясь на более легкие, неконденсируемые газы и осаждая больше углерода на уголь.
Как условия процесса определяют результат
«Победитель» в конкуренции между этими реакциями определяется условиями процесса. Контролируя температуру, скорость нагрева и время пребывания, вы можете направлять процесс для максимизации выхода угля, жидкости или газа.
Медленный пиролиз (фокус на биоугле)
При медленном пиролизе низкие температуры (<400°C) и медленные скорости нагрева дают вторичным реакциям достаточно времени для протекания. Эта среда благоприятствует реакциям образования угля и позволяет некоторым парам реполимеризоваться обратно в твердое вещество, максимизируя выход биоугля.
Быстрый пиролиз (фокус на бионефти)
При быстром пиролизе высокие температуры и чрезвычайно быстрые скорости нагрева почти мгновенно разлагают биомассу. Образующиеся пары немедленно удаляются и охлаждаются (закаляются), чтобы остановить вторичные реакции. Это «замораживает» процесс на промежуточной стадии, максимизируя сбор конденсируемых паров в виде бионефти.
Газификация (фокус на синтез-газе)
Критически важно отличать пиролиз от газификации. В то время как пиролиз происходит в полном отсутствии кислорода, газификация включает преднамеренное введение реактивного агента, такого как кислород, пар или воздух.
Введение окислителя при высоких температурах способствует реакциям образования газа, таким как частичное сгорание (C + ½O₂ → CO) и вышеупомянутые реакции водяного газа. Это принципиально смещает цель в сторону максимизации выхода синтез-газа (CO + H₂).
Понимание компромиссов
Химия пиролиза представляет собой неизбежную «продуктовую трилемму»: невозможно одновременно максимизировать выход угля, масла и газа из одного процесса.
Внутренний продуктовый конфликт
Оптимизация для одного продукта происходит за счет других. Длительное время пребывания, благоприятствующее образованию угля, уничтожит выходы жидкости, поскольку пары крекируются или реполимеризуются. Быстрое охлаждение для сохранения бионефти предотвращает полное протекание вторичных газообразующих реакций.
Сложность биомассы
Биомасса не является однородным химическим веществом. Ее компоненты — целлюлоза, гемицеллюлоза и лигнин — разлагаются при разных температурах и производят разные промежуточные продукты. Эта внутренняя изменчивость означает, что точный контроль и прогнозирование путей реакции остаются значительной технической проблемой.
Оптимизация реакций для вашей цели
Выбор условий пиролиза должен определяться желаемым конечным продуктом. Основные реакции дают четкую дорожную карту для достижения вашей цели.
- Если ваша основная цель — максимизация биоугля: Используйте медленный пиролиз с более низкими температурами (~400°C) и длительным временем пребывания, чтобы способствовать образованию твердых веществ.
- Если ваша основная цель — максимизация бионефти: Используйте быстрый пиролиз с быстрыми скоростями нагрева (>100°C/с), умеренными температурами (~500°C) и коротким временем пребывания паров с последующим быстрым охлаждением.
- Если ваша основная цель — максимизация синтез-газа: Перейдите от пиролиза к газификации, работая при более высоких температурах (>700°C) и вводя такой агент, как пар или воздух, для стимулирования газообразующих реакций.
Понимание этих путей реакции является ключом к превращению сырой биомассы в ценные, индивидуальные продукты.
Сводная таблица:
| Стадия реакции | Ключевой процесс | Основные продукты |
|---|---|---|
| Стадия 1: Первичное разложение | Термическое крекирование целлюлозы, гемицеллюлозы и лигнина в бескислородной среде. | Твердый уголь, первичные пары (смола), неконденсируемые газы (CO, CO₂, H₂) |
| Стадия 2: Вторичные реакции | Уголь и пары вступают в дальнейшие реакции (например, водяной газ, Будуар, крекинг). | Конечный биоуголь, бионефть и синтез-газ |
| Контролирующий фактор | Условия процесса (температура, скорость нагрева, время пребывания) | Определяет конечный выход продукта |
Готовы освоить свой процесс пиролиза?
Понимание сложных реакций — это первый шаг; точный контроль — ключ к успеху. KINTEK специализируется на передовом лабораторном оборудовании и расходных материалах для исследований и анализа биомассы.
Независимо от того, разрабатываете ли вы процесс для максимизации биоугля для улучшения почвы, бионефти для возобновляемого топлива или синтез-газа для энергии, правильное оборудование обеспечивает точный контроль температуры и управление реакциями.
Пусть опыт KINTEK поддержит миссию вашей лаборатории:
- Достижение точного контроля: Оптимизируйте температуру и скорость нагрева, чтобы направлять вторичные реакции к желаемому продукту.
- Повышение точности исследований: Надежные печи и реакторы для воспроизводимых результатов в исследованиях пиролиза.
- Масштабируйте свои инновации: От лабораторных экспериментов до разработки процессов.
Свяжитесь с нами сегодня, чтобы обсудить, как наши решения могут помочь вам раскрыть весь потенциал пиролиза биомассы для вашего конкретного применения.
#КонтактнаяФорма для получения персональной консультации!
Визуальное руководство
Связанные товары
- Электрическая роторная печь для пиролиза биомассы
- Электрическая вращающаяся печь для пиролиза, установка, машина, кальцинатор, малая вращающаяся печь, вращающаяся печь
- Электрическая вращающаяся печь непрерывного действия, малая вращающаяся печь, установка для пиролиза с нагревом
- Настраиваемые лабораторные реакторы высокого давления и высокой температуры для различных научных применений
- Автоклавный реактор для гидротермального синтеза высокого давления
Люди также спрашивают
- Что такое роторный печной реактор? Руководство по промышленной термической обработке
- При какой температуре происходит пиролиз? Руководство по контролю выхода вашей продукции
- Какие реакторы используются для быстрого пиролиза? Выбор правильной системы для максимального выхода био-масла
- Какие бывают типы кальцинаторов? Руководство по выбору подходящего оборудования для термической обработки
- Какова температура вращающейся печи? Это зависит от вашего материала и цели процесса







