Нет, графит не является металлом, но он является превосходным проводником электричества. Это различие часто вызывает путаницу, поскольку нас часто учат ассоциировать проводимость исключительно с металлическими элементами. Графит — это аллотроп — особая структурная форма — неметаллического элемента углерода.
Основная причина этой путаницы заключается в том, что мы склонны группировать материалы по простым категориям, а не по их фундаментальной структуре. Графит, будучи неметаллом, проводит электричество, потому что его уникальное слоистое атомное расположение создает «свободные» электроны, которые ведут себя почти так же, как электроны в настоящем металле.

Что такое графит? Уникальная форма углерода
Свойства графита напрямую вытекают из его уникальной атомной структуры. Понимание этой структуры является ключом к пониманию его поведения.
Не металл, а аллотроп
Элементы могут существовать в различных физических формах, называемых аллотропами. Эти формы состоят из одних и тех же атомов, но имеют разное структурное расположение, что придает им совершенно разные свойства.
Графит — это аллотроп углерода. Самым известным другим аллотропом углерода является алмаз. Хотя и то, и другое — чистый углерод, их структуры делают графит мягким проводником, а алмаз — твердым изолятором.
Структура из наложенных слоев
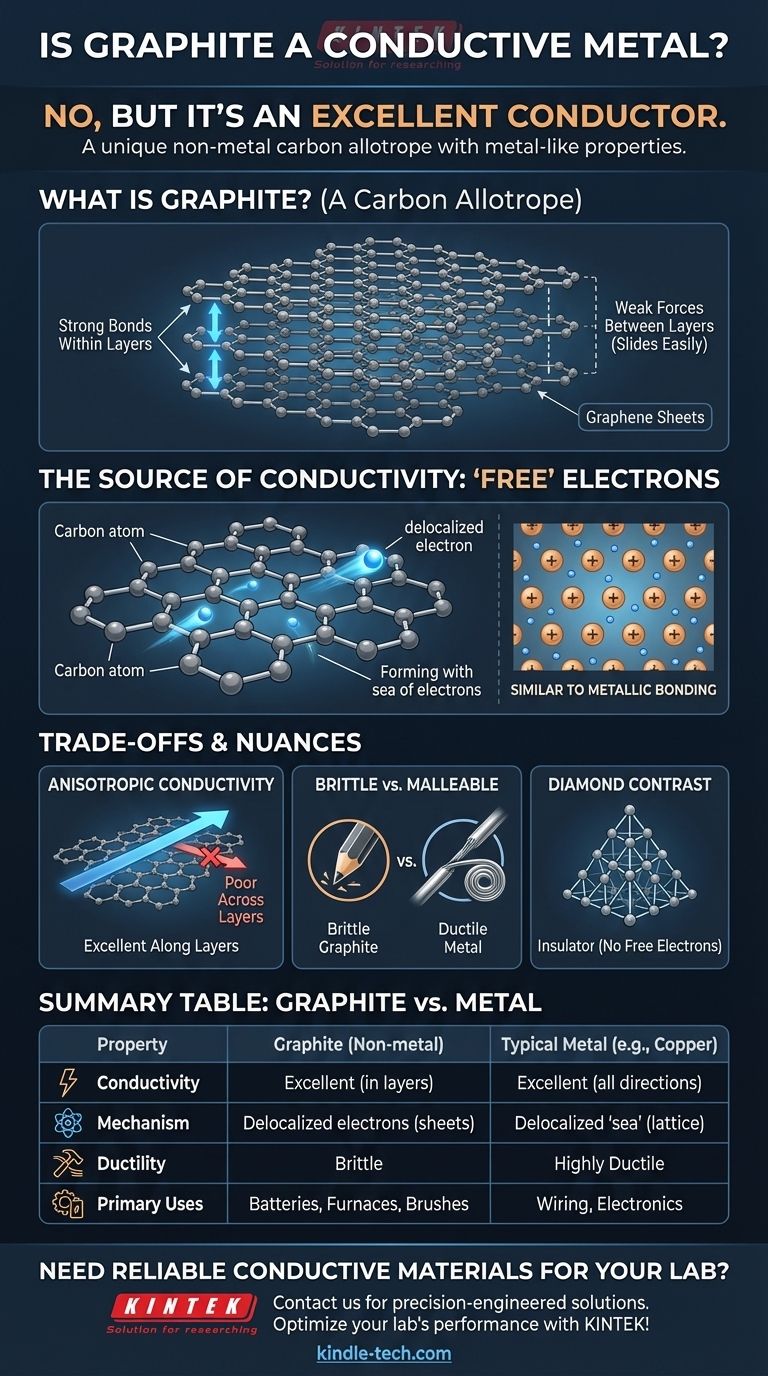
Графит состоит из бесчисленных плоских листов, уложенных друг на друга. Каждый лист, известный как графен, представляет собой одноатомный слой атомов углерода, расположенных в гексагональной решетке, похожей на пчелиные соты.
Связи, удерживающие атомы вместе внутри листа, невероятно прочны. Однако силы, удерживающие различные листы друг с другом, очень слабы, что позволяет им легко скользить друг относительно друга. Вот почему графит мягкий и слоистый, образуя «грифель» в карандашах.
Источник проводимости графита
Причина, по которой графит проводит электричество, кроется в том, как его электроны разделяются — или, вернее, не разделяются. Это имитирует механизм проводимости металлов, хотя графит сам по себе не является металлом.
Роль электронов углерода
Каждый атом углерода имеет четыре внешних электрона (валентных электрона), доступных для образования связей. В гексагональной структуре графенового листа каждый атом углерода образует прочные ковалентные связи с тремя соседними атомами.
«Свободный» делокализованный электрон
Это оставляет один из четырех валентных электронов неучтенным. Этот четвертый электрон не заблокирован в связи между двумя конкретными атомами. Вместо этого он становится делокализованным, свободным перемещаться в любом месте вдоль своего двумерного графенового листа.
«Море электронов» в неметалле
Эта совокупность делокализованных электронов образует подвижное «море электронов» внутри каждого слоя. Поскольку электрический ток — это просто поток электронов, эти свободно движущиеся электроны позволяют графиту легко проводить электричество.
Это фундаментально похоже на металлическую связь, где решетка положительных ионов металла находится в «море» общих, делокализованных электронов. Графит достигает аналогичного результата, используя совершенно другую атомную структуру.
Понимание компромиссов и нюансов
Хотя графит является проводником, он не является идеальной заменой металлам. Его неметаллическая природа сопряжена с явными компромиссами.
Проводимость не является однородной
Графит сильно анизотропен, что означает, что его свойства зависят от направления. Он чрезвычайно хорошо проводит электричество вдоль своих графеновых листов, но очень плохо поперек них. Большинство металлов, напротив, изотропны и проводят электричество одинаково хорошо во всех направлениях.
Хрупкость против ковкости
Металлы, как правило, тянутся и пластичны, что означает, что их можно вытягивать в проволоку или выковывать в новые формы без разрушения. Графит хрупок и разрушится при аналогичной нагрузке. Вы не можете сформировать графитовую проволоку, растягивая ее.
Алмаз: Изолирующий аналог
Алмаз представляет собой идеальный контраст. В своей жесткой тетраэдрической решетке каждый атом углерода связан с четырьмя другими, используя все четыре валентных электрона. Без делокализованных электронов нет ничего свободного для перемещения и переноса тока, что делает алмаз превосходным электрическим изолятором.
Выбор правильного материала для вашего применения
Понимание этих принципов позволяет вам выбрать правильный материал в зависимости от конкретных свойств, необходимых для задачи.
- Если ваш основной акцент делается на гибкой, всенаправленной проводимости: Металлы, такие как медь и алюминий, остаются лучшим выбором благодаря их пластичности и изотропной природе.
- Если ваш основной акцент делается на легком, химически стабильном проводнике для высоких температур: Графит является идеальным материалом для таких применений, как электроды батарей, футеровка печей и щетки электродвигателей.
- Если ваш основной акцент делается на твердости и электрической изоляции: Решением является алмаз, другой известный аллотроп углерода, что доказывает, что атомное расположение определяет все.
В конечном счете, свойства материала определяются его атомной структурой, а не простой категорией, в которую мы его помещаем.
Сводная таблица:
| Свойство | Графит | Типичный металл (например, медь) |
|---|---|---|
| Тип материала | Неметалл (аллотроп углерода) | Металл |
| Электропроводность | Отличная (внутри слоев) | Отличная (во всех направлениях) |
| Механизм проводимости | Делокализованные электроны в графеновых слоях | Делокализованное «море электронов» |
| Пластичность/Ковкость | Хрупкий, нельзя вытянуть в проволоку | Высокопластичный и ковкий |
| Основные области применения | Батареи, футеровка печей, моторные щетки | Проводка, конструкционные элементы, электроника |
Нужен надежный проводящий материал для вашего лабораторного применения? Независимо от того, работаете ли вы с высокотемпературными печами, исследованиями батарей или настраиваемыми электродными установками, опыт KINTEK в области лабораторного оборудования и расходных материалов гарантирует, что вы получите правильное решение. Наша команда поможет вам выбрать материалы, соответствующие вашим конкретным требованиям к проводимости, температуре и долговечности. Свяжитесь с нами сегодня, чтобы оптимизировать производительность вашей лаборатории с помощью точно спроектированных решений от KINTEK!
Визуальное руководство
Связанные товары
- Графитовая вакуумная печь для графитации пленки с высокой теплопроводностью
- Графитовый дисковый стержневой и листовой электрод Электрохимический графитовый электрод
- Графитировочная печь сверхвысоких температур в вакууме
- Графитовый тигель высокой чистоты для испарения
- Углеграфитовая пластина, изготовленная методом изостатического прессования
Люди также спрашивают
- Какова температура графитовой печи? Достижение экстремального тепла до 3000°C
- Каковы интерференции печи Грифеля? Преодоление матричных и спектральных проблем для точного ГФААС
- Каковы недостатки графитовых печей? Ключевые ограничения и эксплуатационные расходы
- Каков температурный диапазон графитовой печи? Достигайте до 3000°C для обработки передовых материалов.
- Что делает графитовая печь? Достижение экстремального нагрева и сверхчувствительного анализа












