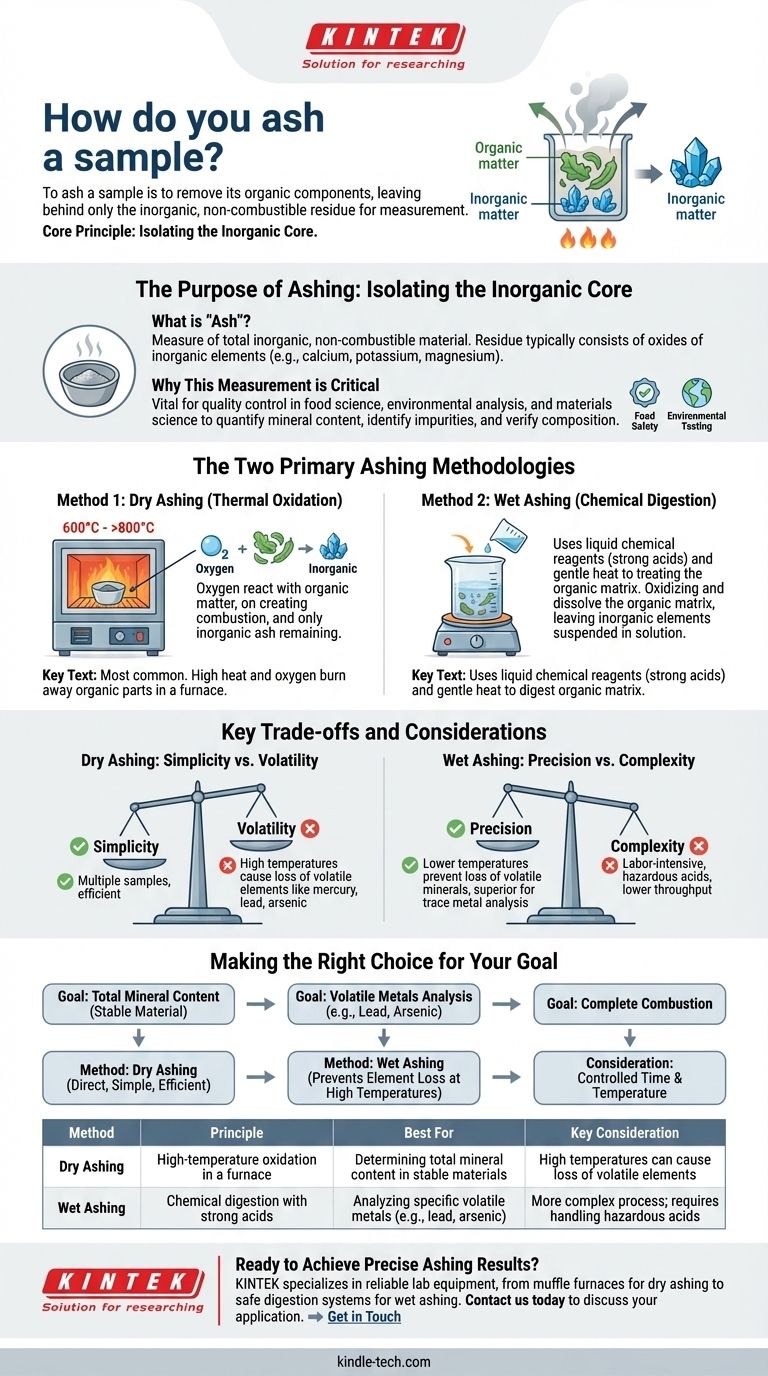
Прокаливание образца означает удаление его органических компонентов, оставляя только неорганический, негорючий остаток для измерения. Наиболее распространенный метод включает помещение образца в высокотемпературную печь и нагревание его в присутствии воздуха до тех пор, пока вся органическая материя не сгорит в результате окисления.
Основной принцип прокаливания — полное отделение органического и неорганического вещества. Выбор метода — либо высокотемпературное сухое прокаливание, либо химическое мокрое прокаливание — определяется конкретными элементами, которые вам необходимо измерить, и их стабильностью.

Цель прокаливания: Выделение неорганического ядра
Прокаливание — это фундаментальная аналитическая техника, используемая для определения минерального или неорганического содержания образца. Полученный озол представляет собой концентрированную форму этих компонентов для дальнейшего анализа.
Что такое «Зола»?
Содержание золы — это мера общего количества неорганического, негорючего материала в образце. Этот остаток обычно состоит из оксидов неорганических элементов (таких как кальций, калий, магний и т. д.), которые присутствовали в исходном материале.
Почему это измерение критически важно
Определение содержания золы жизненно важно для контроля качества во многих отраслях, включая пищевую науку, экологический анализ и материаловедение. Это помогает количественно оценить содержание минералов, выявить примеси или проверить состав продукта.
Две основные методологии прокаливания
Хотя оба метода достигают одной и той же цели — удаления органического материала — они работают на совершенно разных принципах.
Метод 1: Сухое прокаливание (Термическое окисление)
Сухое прокаливание является наиболее распространенным подходом. Он использует высокую температуру и кислород для сжигания органических частей образца.
Подготовленный образец помещают в тигель, который затем нагревают в муфельной печи. По мере повышения температуры органические соединения вступают в реакцию с кислородом в воздухе и сгорают, оставляя позади только неорганическую золу.
Метод 2: Мокрое прокаливание (Химическое разложение)
Мокрое прокаливание, также известное как кислотное разложение, использует жидкие химические реагенты вместо высокой температуры.
Этот процесс включает добавление сильных кислот к образцу и его мягкое нагревание. Кислоты агрессивно окисляют и растворяют органическую матрицу, оставляя неорганические элементы во взвешенном состоянии в полученном растворе.
Ключевые компромиссы и соображения
Выбор неправильного метода может привести к неточным результатам. Решение зависит от компромисса между простотой и возможностью потери определяемого вещества.
Сухое прокаливание: Простота против летучести
Основное преимущество сухого прокаливания — его простота и возможность обрабатывать несколько образцов одновременно.
Однако высокие температуры (часто от 600°C до более 800°C) могут привести к испарению и потере некоторых летучих неорганических элементов, таких как ртуть, свинец или мышьяк. Это делает его непригодным для анализа этих конкретных элементов.
Мокрое прокаливание: Точность против сложности
Мокрое прокаливание проводится при гораздо более низких температурах, что предотвращает потерю летучих минералов. Это делает его лучшим выбором для анализа следовых металлов.
Недостатком является то, что это более сложный, трудоемкий процесс. Он требует осторожного обращения с опасными кислотами и имеет гораздо меньшую пропускную способность образцов по сравнению с сухим прокаливанием.
Принятие правильного решения для вашей цели
Ваша аналитическая цель диктует правильную процедуру прокаливания.
- Если ваша основная цель — определение общего содержания минералов в стабильном материале: Сухое прокаливание является наиболее прямым, простым и эффективным методом.
- Если ваша основная цель — анализ на наличие специфических летучих металлов (например, свинца или мышьяка): Мокрое прокаливание необходимо для предотвращения потери этих элементов при высоких температурах.
- Если ваша цель — обеспечение полного сгорания: Время и температура прокаливания должны тщательно контролироваться, чтобы они были достаточно долгими для удаления всех органических веществ, но не настолько долгими, чтобы изменить неорганический остаток.
В конечном счете, выбор правильной техники прокаливания является критически важным первым шагом, который полностью зависит от состава вашего образца и конкретных элементов, которые вы намерены измерить.
Сводная таблица:
| Метод | Принцип | Лучше всего подходит для | Ключевое соображение |
|---|---|---|---|
| Сухое прокаливание | Высокотемпературное окисление в печи | Определение общего содержания минералов в стабильных материалах | Высокие температуры могут вызвать потерю летучих элементов |
| Мокрое прокаливание | Химическое разложение сильными кислотами | Анализ специфических летучих металлов (например, свинца, мышьяка) | Более сложный процесс; требует работы с опасными кислотами |
Готовы получить точные результаты прокаливания?
Выбор правильного метода прокаливания имеет решающее значение для точного неорганического анализа. KINTEK специализируется на предоставлении надежного лабораторного оборудования — от прочных муфельных печей для сухого прокаливания до безопасных систем разложения для мокрого прокаливания, — которое необходимо вашей лаборатории для получения стабильных, высококачественных результатов.
Свяжитесь с нами сегодня, чтобы обсудить ваше конкретное применение, и позвольте нашим экспертам помочь вам выбрать идеальное решение. ➡️ Связаться с нами
Визуальное руководство