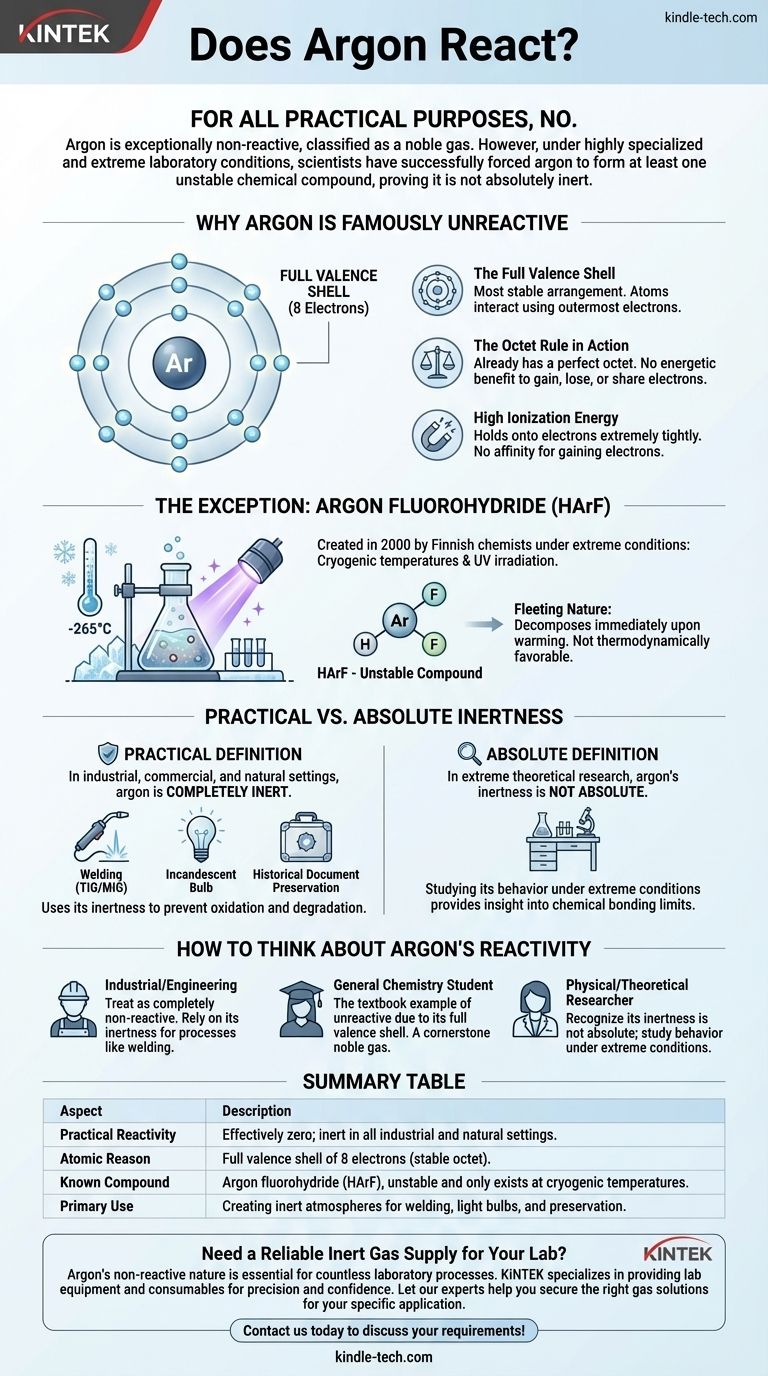
Для всех практических целей — нет. Аргон исключительно нереактивен, поэтому он классифицируется как благородный газ. Однако в высокоспециализированных и экстремальных лабораторных условиях ученым удалось принудительно заставить аргон образовать по крайней мере одно нестабильное химическое соединение, доказав, что он не является абсолютно инертным.
Основной вывод заключается в том, что «реакционная способность» элемента — это не простой вопрос «да» или «нет». Хотя идеальная конфигурация электронной оболочки аргона делает его инертным в любом естественном или промышленном контексте, его нереактивность может быть преодолена достаточной энергией в криогенных условиях, что раскрывает тонкие сложности химической связи.

Почему аргон известен как "нереактивный"
Чтобы понять, почему аргон так сильно сопротивляется образованию химических связей, мы должны рассмотреть его атомную структуру. Его репутация инертного газа не случайна; это прямой результат его электронной конфигурации.
Полная валентная оболочка
Атомы взаимодействуют и образуют связи, используя свои внешние электроны, известные как валентные электроны.
Аргон имеет восемь валентных электронов, что полностью заполняет его внешнюю электронную оболочку. Это наиболее стабильное расположение, которое может иметь атом.
"Правило октета" в действии
"Правило октета" — это фундаментальный принцип в химии, который гласит, что атомы стремятся приобрести, потерять или разделить электроны, чтобы достичь полной внешней оболочки из восьми электронов.
Поскольку аргон уже имеет этот идеальный октет, для него нет энергетической выгоды в приобретении, потере или разделении электронов с другими атомами. Он уже находится в своем идеальном, низкоэнергетическом состоянии.
Высокая энергия ионизации
Энергия ионизации — это энергия, необходимая для удаления электрона из атома. Аргон имеет очень высокую энергию ионизации, что означает, что он очень крепко удерживает свои электроны.
Аналогично, он не имеет сродства к приобретению электронов. Просто нет химического "мотива" для аргона вступать в реакцию в нормальных условиях.
Исключение, которое подтверждает правило
В течение десятилетий аргон считался полностью инертным. Это изменилось в 2000 году, когда команда финских химиков создала первое известное истинное соединение аргона.
Принуждение к реакции в экстремальных условиях
Соединение, фторогидрид аргона (HArF), не было создано в обычном лабораторном стакане.
Ученым пришлось заморозить смесь аргона и фтороводорода на поверхности при температурах, близких к абсолютному нулю (около -265°C или -445°F), а затем облучить ее мощным ультрафиолетовым светом. Этого экстремального энергетического воздействия было достаточно, чтобы временно заставить неохотный атом аргона образовать связь.
Мимолетная природа соединений аргона
Полученное соединение HArF невероятно нестабильно. Оно существует только при этих криогенных температурах.
Если его немного нагреть, слабые связи разрываются, и оно немедленно разлагается обратно на отдельные аргон и фтороводород. Это подчеркивает, что соединение не является термодинамически выгодным и существует только потому, что оно "заперто" экстремальным холодом.
Практическая инертность против абсолютной инертности
Это открытие заставляет нас различать две концепции: то, что верно в практическом смысле, и то, что верно в абсолютном, теоретическом смысле.
Практическое определение инертности
В любой промышленной, коммерческой или природной среде аргон полностью инертен. Он не реагирует с воздухом, водой, металлами или любым другим веществом, с которым контактирует.
Именно эта практическая инертность делает его таким ценным.
Почему это важно для применений
Нереактивность аргона — это особенность, а не ограничение. При сварке (TIG/MIG) он создает инертный "щит" вокруг расплавленного металла, предотвращая его окисление или реакцию с газами в воздухе, что обеспечивает чистый, прочный шов.
В лампах накаливания светящихся ламп атмосфера аргона предотвращает выгорание горячей вольфрамовой нити. При сохранении исторических документов он обеспечивает бескислородную среду для предотвращения деградации.
Как понимать реакционную способность аргона
Ваш контекст определяет, как вы должны рассматривать химическое поведение аргона. Понимание этого различия является ключом к правильному применению химических принципов.
- Если вы работаете в промышленной или инженерной среде: Считайте аргон полностью нереактивным газом. Его инертность является его наиболее ценным свойством, и на нее можно полагаться в таких процессах, как сварка и производство.
- Если вы студент общей химии: Поймите, что аргон является хрестоматийным примером нереактивного элемента благодаря его полностью заполненной валентной электронной оболочке, что делает его краеугольным камнем группы благородных газов.
- Если вы исследователь в области физической или теоретической химии: Признайте, что инертность аргона не является абсолютной, и изучение его поведения в экстремальных условиях дает ценное представление о пределах химической связи.
В конечном итоге, крайняя нежелание аргона вступать в реакцию является фундаментальным свойством, которое делает его как научно интересным, так и чрезвычайно полезным в реальном мире.
Сводная таблица:
| Аспект | Описание |
|---|---|
| Практическая реакционная способность | Практически нулевая; инертен во всех промышленных и природных условиях. |
| Атомная причина | Полная валентная оболочка из 8 электронов (стабильный октет). |
| Известное соединение | Фторогидрид аргона (HArF), нестабилен и существует только при криогенных температурах. |
| Основное применение | Создание инертных атмосфер для сварки, ламп накаливания и консервации. |
Нужен надежный источник инертного газа для вашей лаборатории?
Нереактивная природа аргона необходима для бесчисленных лабораторных процессов, от создания контролируемых атмосфер до работы с чувствительными материалами. Обеспечение постоянного, высокочистого снабжения имеет решающее значение для ваших результатов.
KINTEK специализируется на предоставлении лабораторного оборудования и расходных материалов, необходимых для точной и уверенной работы. Позвольте нашим экспертам помочь вам подобрать правильные газовые решения для вашего конкретного применения.
Свяжитесь с нами сегодня через нашу форму, чтобы обсудить ваши требования!
Визуальное руководство