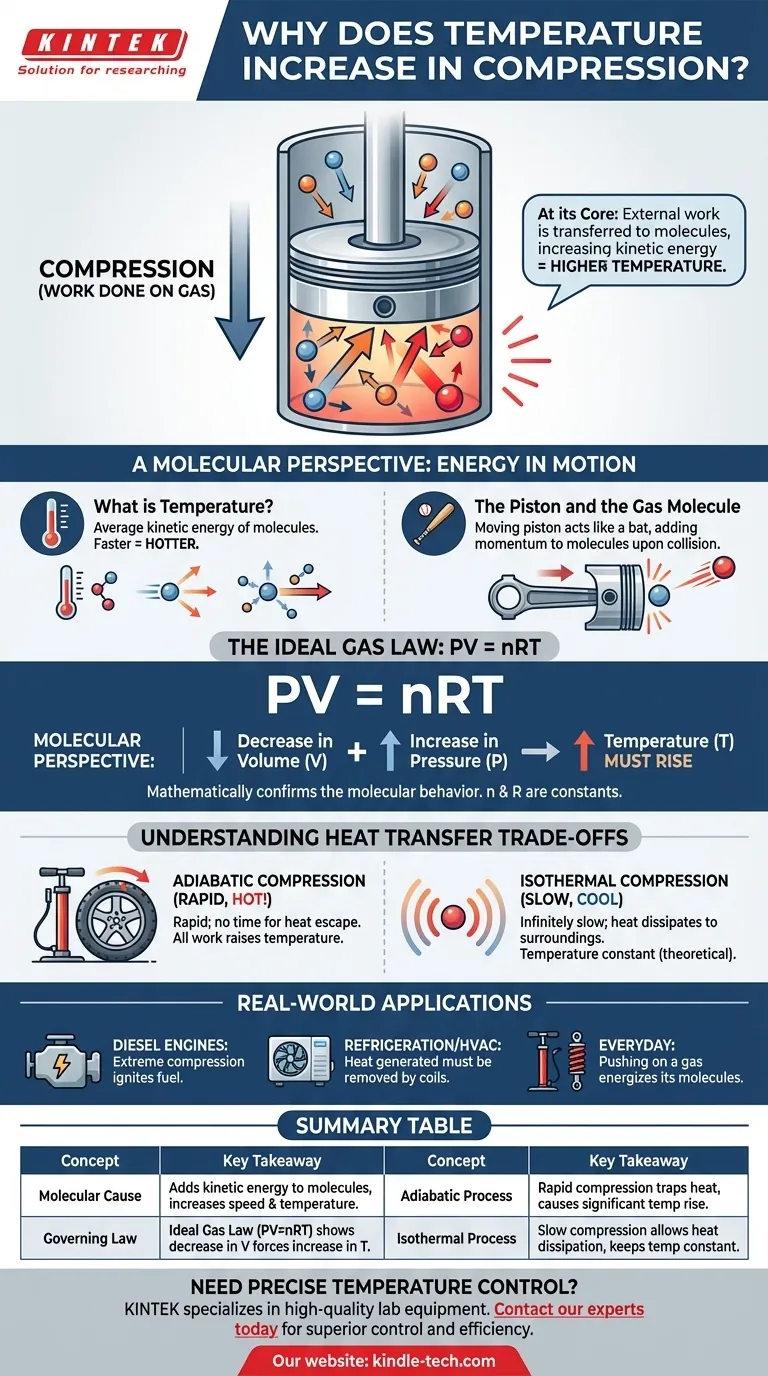
По своей сути, сжатие газа увеличивает его температуру, потому что вы совершаете над ним работу. Эта внешняя работа напрямую передается молекулам газа, увеличивая их кинетическую энергию. Мы измеряем это увеличение средней кинетической энергии молекул как повышение температуры.
Акт сжатия — это не просто уменьшение объема; это вливание энергии. Сила, которую вы прикладываете для сжатия газа, добавляет энергии его молекулам, заставляя их двигаться быстрее, что мы воспринимаем как тепло.

Молекулярная перспектива: энергия в движении
Чтобы по-настоящему понять нагрев при сжатии, мы должны подумать о том, что происходит на уровне отдельных молекул. Температура газа — это просто мера среднего движения его бесчисленных частиц.
Что такое температура на самом деле?
Температура — это макроскопическое измерение средней кинетической энергии молекул в системе. Более быстро движущиеся молекулы обладают большей кинетической энергией, что приводит к более высокой температуре. Более медленно движущиеся молекулы означают более низкую температуру.
Акт сжатия
Представьте газ, заключенный в цилиндре с подвижным поршнем. Чтобы сжать газ, вы должны физически толкать поршень внутрь, прикладывая силу на расстоянии. Это действие является научным определением работы.
Поршень и молекула газа
Представьте себе движущийся поршень как биту, а молекулу газа — как мяч. Когда молекула сталкивается со стационарным поршнем, она отскакивает с той же скоростью. Однако, когда она сталкивается с поршнем, движущимся внутрь, поршень придает импульс и энергию молекуле, заставляя ее отскакивать с большей скоростью.
Совокупный эффект
Этот перенос энергии происходит миллиарды раз в секунду со всеми молекулами, ударяющимися о поверхность поршня. Каждое столкновение добавляет крошечное количество энергии. Совокупный результат — значительное увеличение средней скорости — а следовательно, и средней кинетической энергии — всей популяции молекул, что вызывает повышение температуры газа.
Роль закона идеального газа
Это молекулярное поведение математически описывается фундаментальными законами физики, проще всего — Законом идеального газа. Он обеспечивает высокоуровневое подтверждение того, что мы видим на молекулярном уровне.
Управляющее уравнение: PV = nRT
Закон идеального газа связывает давление (P), объем (V) и температуру (T) заданного количества газа (n). «R» — это константа. Это уравнение показывает, что эти свойства внутренне связаны.
Как закон предсказывает результат
Когда вы сжимаете газ, вы уменьшаете его объем (V). Приложенная вами сила также увеличивает его давление (P). Чтобы уравнение PV = nRT оставалось сбалансированным, увеличение левой части уравнения (из-за комбинации увеличения P и уменьшения V) должно компенсироваться увеличением правой части. Поскольку n и R постоянны, температура (T) должна расти.
Понимание компромиссов: теплопередача
Скорость сжатия кардинально меняет результат, поскольку она определяет, сколько времени система имеет для взаимодействия с окружающей средой.
Адиабатическое сжатие (тепло не уходит)
Это происходит, когда сжатие настолько быстрое, что нет времени для выделяющегося тепла, чтобы уйти в окружающую среду. Вся совершаемая вами работа напрямую преобразуется в повышение внутренней энергии и температуры газа. Накачивание велосипедной шины — близкий пример из реальной жизни; насос заметно нагревается.
Изотермическое сжатие (идеальный отвод тепла)
Это теоретический идеал, который возникает, когда сжатие происходит бесконечно медленно. Такой медленный темп позволяет всему дополнительному теплу, выделяемому работой, рассеиваться в окружающую среду, сохраняя температуру газа постоянной. Хотя это практически недостижимо, это критически важная концепция для термодинамического анализа.
Сценарий реального мира
Почти все процессы в реальном мире находятся между этими двумя крайностями. Часть совершаемой работы увеличивает внутреннюю температуру, в то время как часть выделяемого тепла теряется в окружающей среде.
Как применить этот принцип
Понимание нагрева при сжатии — это не просто академический вопрос; это основа бесчисленных практических применений и систем.
- Если ваше основное внимание уделяется повседневным явлениям: Помните, что давление на газ (совершение работы) заряжает его молекулы энергией, поэтому велосипедный насос или амортизатор нагреваются.
- Если ваше основное внимание уделяется конструкции двигателей: Этот принцип является самой основой дизельного двигателя, который использует сильное сжатие для нагрева воздуха до такой степени, чтобы воспламенить топливо без свечи зажигания.
- Если ваше основное внимание уделяется холодильному оборудованию или системам ОВКВ: Тепло, выделяющееся на этапе сжатия хладагента, является отработанным теплом, которое должно активно отводиться конденсаторными змеевиками на задней стороне вашего холодильника или в наружном блоке кондиционера.
В конечном счете, связь между механической работой и тепловой энергией является фундаментальным законом физики, преобразующим силу в тепло на молекулярном уровне.
Сводная таблица:
| Концепция | Ключевой вывод |
|---|---|
| Молекулярная причина | Сжатие добавляет кинетическую энергию молекулам газа, увеличивая их скорость и температуру. |
| Управляющий закон | Закон идеального газа (PV=nRT) математически показывает, что уменьшение объема (V) вынуждает температуру (T) расти. |
| Адиабатический процесс | Быстрое сжатие (например, велосипедный насос) задерживает тепло, вызывая значительное повышение температуры. |
| Изотермический процесс | Медленное, теоретическое сжатие позволяет теплу рассеиваться, сохраняя температуру постоянной. |
| Влияние на реальный мир | Основа для дизельных двигателей, холодильных циклов и систем ОВКВ. |
Нужен точный контроль температуры для ваших процессов? Принципы термодинамики имеют решающее значение для исследований и разработок, а также для промышленных применений. KINTEK специализируется на высококачественном лабораторном оборудовании и расходных материалах, удовлетворяя взыскательные потребности лабораторий. Независимо от того, разрабатываете ли вы новые материалы или оптимизируете тепловые системы, наш опыт может поддержать вашу работу. Свяжитесь с нашими экспертами сегодня, чтобы обсудить, как мы можем помочь вам достичь превосходного контроля и эффективности в вашей лаборатории.
Визуальное руководство
Связанные товары
Люди также спрашивают
- Как выбрать лучший пластинчато-роторный насос для конкретных нужд? Сопоставьте требования вашего применения
- Как работает роторный пластинчатый насос? Откройте для себя эффективные вакуумные технологии для вашей лаборатории
- Как сравниваются характеристики одноступенчатых и двухступенчатых пластинчато-роторных насосов? Оптимизируйте эффективность вакуума
- Каковы основные недостатки роторных пластинчатых насосов? Избегайте загрязнения и высоких затрат на техническое обслуживание
- Почему пластинчато-роторный насос часто называют «форвакуумным насосом»? Понимание его критической роли в вакуумных системах
