По сути, электролитическая ячейка — это устройство, которое использует электрическую энергию для осуществления химической реакции, которая в противном случае не произошла бы сама по себе. Она работает путем пропускания электрического тока через вещество, обычно раствор, содержащий ионы, для его разложения или преобразования. Ключевые промышленные применения включают производство водорода из воды, очистку металлов, таких как медь, и производство основных химикатов, таких как хлор и гидроксид натрия.
Электролитическая ячейка фундаментально преобразует электрическую энергию в химическую энергию. Она преодолевает естественную стабильность соединений, используя электричество в качестве инструмента для их расщепления и создания новых, часто более ценных веществ.

Как работает электролитическая ячейка
Электролитическая ячейка работает по принципу электролиза, что буквально означает «расщепление с помощью электричества». Этот процесс противоположен тому, что происходит в батарее (гальваническом элементе), которая производит электричество из спонтанной химической реакции.
Основной принцип: принуждение к реакции
Многие ценные химические соединения, такие как вода (H₂O) или соль (NaCl), очень стабильны. Они не распадаются спонтанно на свои составные элементы.
Электролитическая ячейка обеспечивает необходимую энергию в виде внешнего напряжения, чтобы заставить эти несамопроизвольные реакции произойти. Этот ввод энергии преодолевает химические связи, удерживающие соединение вместе.
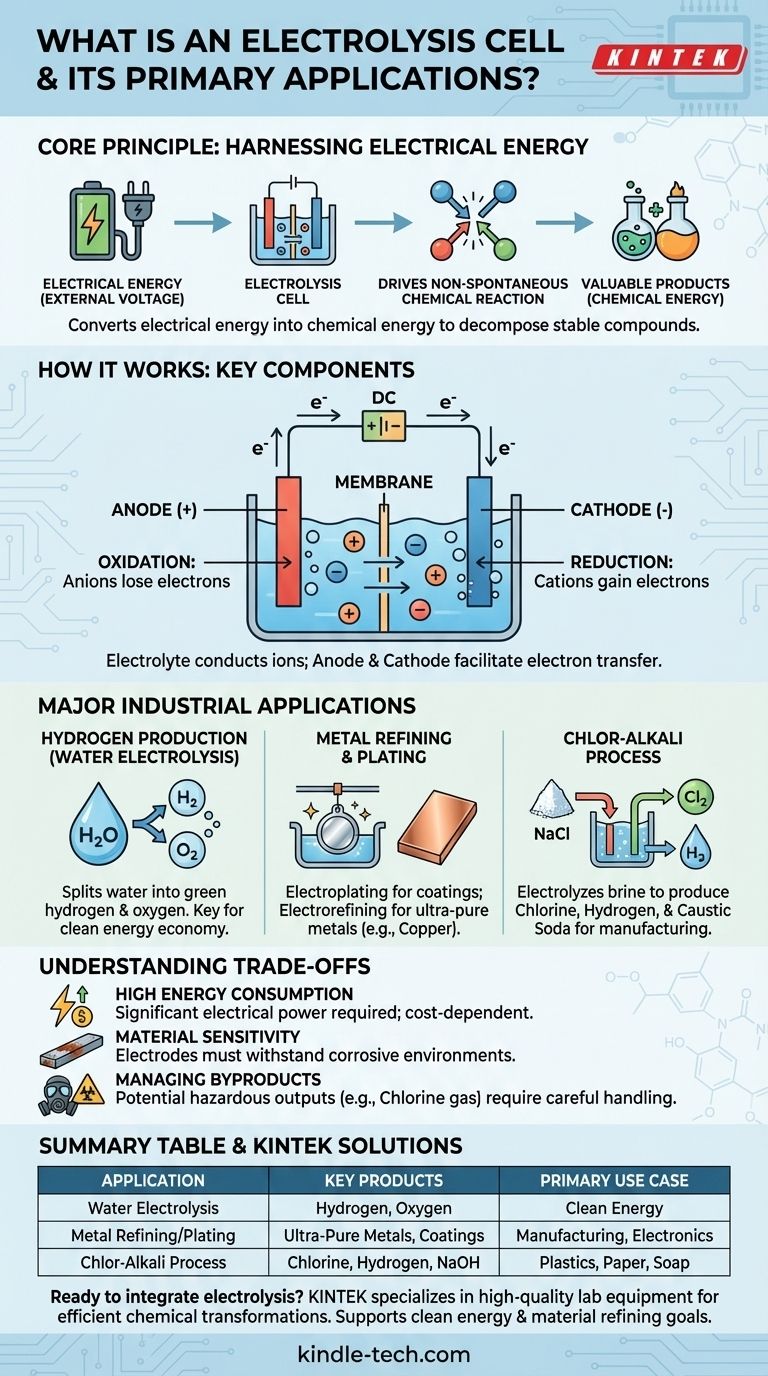
Ключевые компоненты
Каждая электролитическая ячейка имеет три основных компонента:
- Анод: Положительный электрод. На аноде отрицательно заряженные ионы (анионы) теряют электроны в процессе, называемом окислением.
- Катод: Отрицательный электрод. На катоде положительно заряженные ионы (катионы) получают электроны в процессе, называемом восстановлением.
- Электролит: Вещество (часто раствор), содержащее свободно движущиеся ионы. Электролит проводит электричество и является сырьем для реакции.
Тип электродов и используемый электролит тщательно подбираются, поскольку они напрямую определяют, какие продукты будут образованы.
Основные промышленные применения
Способность точно контролировать химические превращения с помощью электричества делает электролиз краеугольным камнем современной промышленности.
Производство водорода из воды
Пожалуй, наиболее обсуждаемым применением сегодня является электролиз воды. Пропуская ток через воду (содержащую подходящий электролит), ячейка расщепляет молекулы H₂O на их компоненты.
Кислородный газ образуется на аноде, а чистый водородный газ — на катоде. Когда используемое электричество поступает из возобновляемых источников, полученный продукт называется «зеленым водородом», ключевым компонентом будущей экономики чистой энергии.
Очистка и гальванизация металлов
Электролиз имеет решающее значение для производства и очистки металлов. При гальванизации объект помещается в качестве катода в ячейку, содержащую ионы желаемого металла для покрытия (например, хрома или никеля). Ионы металла восстанавливаются на объекте, образуя тонкое, прочное покрытие.
Аналогично, электрорафинирование используется для получения сверхчистых металлов. Например, неочищенная плита меди используется в качестве анода. При подаче тока атомы меди растворяются в электролите, перемещаются к катоду и повторно осаждаются в виде почти 100% чистой меди, оставляя примеси позади.
Хлор-щелочной процесс
Этот масштабный промышленный процесс является одним из наиболее значимых применений электролиза. Электролизу подвергается сильный раствор хлорида натрия (рассол).
Результатом является производство трех очень ценных товарных химикатов из простой соленой воды: газообразного хлора, газообразного водорода и гидроксида натрия (каустической соды). Это основные ингредиенты для производства пластмасс, бумаги, мыла и тысяч других продуктов.
Понимание компромиссов
Хотя электролиз является мощным инструментом, он не является универсальным решением. Его применение сопряжено со значительными соображениями.
Высокое энергопотребление
Основным недостатком электролиза является его высокая потребность в энергии. Для расщепления стабильного соединения требуется значительное количество электроэнергии, что может сделать процесс дорогостоящим. Экономическая целесообразность электролитического процесса часто напрямую связана со стоимостью электроэнергии.
Чувствительность материалов и коррозия
Сами электроды являются частью активной химической среды. Они должны быть способны выдерживать коррозионные условия и высокие температуры без деградации или нежелательных реакций. Выбор правильного материала электрода имеет решающее значение для эффективности и долговечности.
Управление побочными продуктами
Электролиз может производить опасные или трудноутилизируемые побочные продукты. Например, в хлор-щелочном процессе образующийся газообразный хлор токсичен и должен обрабатываться с особой осторожностью. Общее воздействие на окружающую среду сильно зависит как от источника электроэнергии, так и от безопасного обращения со всеми выходами.
Правильный выбор для вашей цели
Конструкция и эксплуатация электролитической ячейки специально адаптированы к ее предполагаемому назначению.
- Если ваша основная цель — производство металлов высокой чистоты: Ваш процесс будет сосредоточен на электрорафинировании или электроэкстракции, где точный контроль напряжения и чистота электролита имеют первостепенное значение для обеспечения качества продукта.
- Если ваша основная цель — производство товарных химикатов: Вы, вероятно, будете использовать модель, подобную хлор-щелочному процессу, которая оптимизирована для непрерывного крупномасштабного производства из недорогого сырья, такого как рассол.
- Если ваша основная цель — создание носителей чистой энергии: Ваши усилия будут включать электролиз воды, где эффективность ячейки и интеграция с недорогими возобновляемыми источниками энергии являются наиболее важными факторами успеха.
Применяя целенаправленную электрическую энергию, электролитическая ячейка преобразует основные исходные материалы в высокоценные продукты, что делает ее фундаментальным инструментом современной химии и промышленности.
Сводная таблица:
| Применение | Ключевые продукты | Основной вариант использования |
|---|---|---|
| Электролиз воды | Водород и кислородный газ | Чистая энергия (зеленый водород) |
| Очистка/покрытие металлов | Сверхчистые металлы, защитные покрытия | Производство, электроника |
| Хлор-щелочной процесс | Хлор, водород, гидроксид натрия | Производство пластмасс, бумаги, мыла |
Готовы интегрировать технологию электролиза в свою лабораторию или промышленный процесс? KINTEK специализируется на высококачественном лабораторном оборудовании и расходных материалах, предоставляя надежные инструменты, необходимые для эффективных и точных химических превращений. Независимо от того, разрабатываете ли вы решения для чистой энергии или очищаете материалы, наш опыт поддерживает ваши цели. Свяжитесь с нашей командой сегодня, чтобы обсудить, как мы можем улучшить ваши операции.
Визуальное руководство
Связанные товары
- Настраиваемые электролизеры PEM для различных исследовательских применений
- Электрохимическая ячейка для спектроэлектролиза в тонком слое
- Электрохимическая ячейка с газодиффузионным электролизом и ячейка для реакции с протоком жидкости
- Кварцевая электрохимическая ячейка для электрохимических экспериментов
- Электрохимическая ячейка из ПТФЭ, коррозионностойкая, герметичная и негерметичная
Люди также спрашивают
- Что такое электролитическая ячейка? Руководство по проведению химических реакций с помощью электричества
- Как еще называют электролитическую ячейку? Понимание электролитических и гальванических ячеек
- Каковы риски неправильного контроля напряжения в электролитической ячейке? Избегайте дорогостоящих повреждений и неэффективности
- Каковы конфигурации отверстий для незапечатанной и запечатанной версий электролитической ячейки? Оптимизируйте вашу электрохимическую установку
- Каковы меры предосторожности при нагревании или стерилизации электролитической ячейки? Избегайте повреждения чувствительных компонентов



















