Иллюзия простоты
В лаборатории самые важные моменты часто самые тихие.
Мы склонны зацикливаться на сложной химии — экзотических реагентах, точном напряжении, теоретическом выходе. Но в электрохимии весь эксперимент зависит от механического действия, которое занимает менее пяти минут: установки электродов.
Это кажется пустяком. Вы помещаете металл в стекло. Включаете питание.
Но такой взгляд опасен.
Электролитическая ячейка — это не просто контейнер; это цепь. Электрод — это интерфейс, где физический мир встречается с химическим миром. Если этот интерфейс имеет дефект — даже на миллиметр — данные не просто немного искажены. Это вымысел.
Вот как подойти к процессу установки с точностью инженера и дисциплиной хирурга.
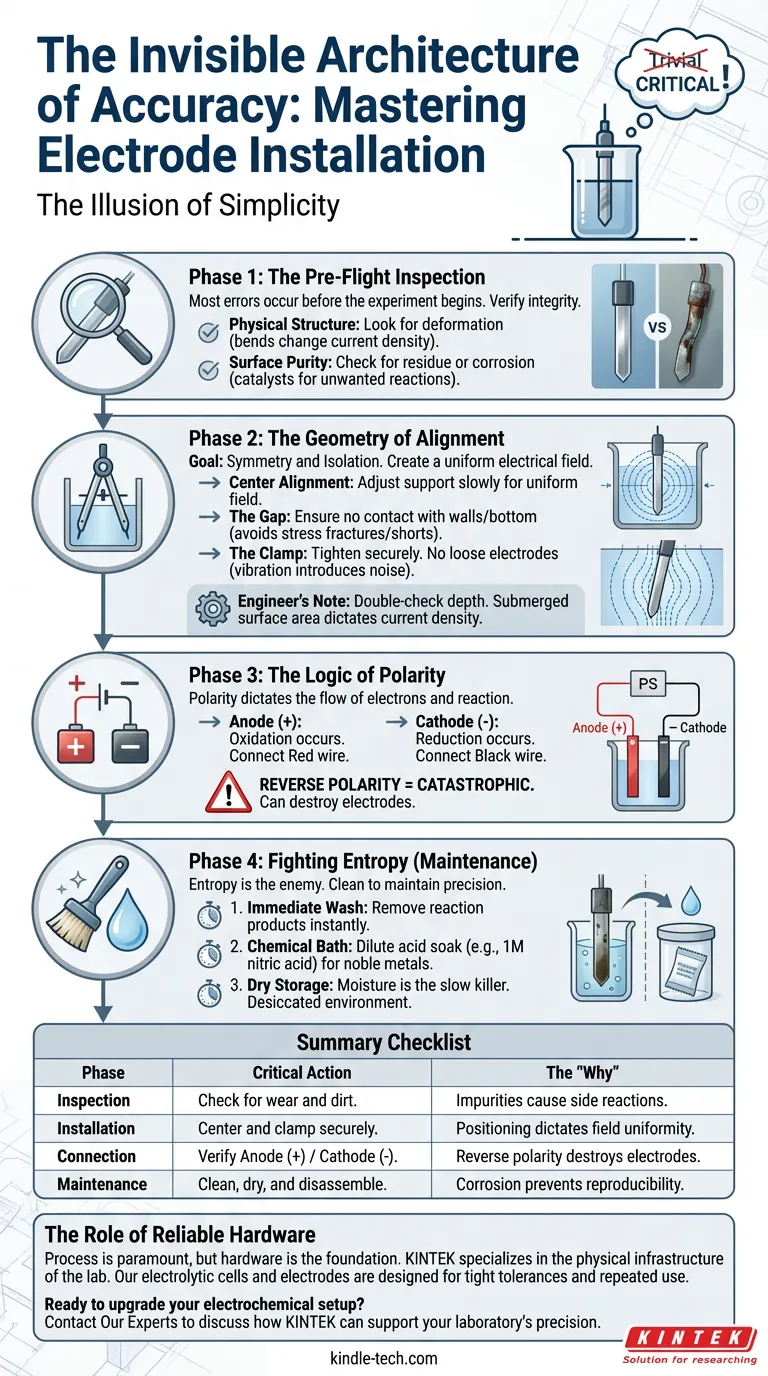
Этап 1: Предстартовая проверка
Большинство ошибок происходит до начала эксперимента.
Мы часто предполагаем, что раз электрод выглядит целым, он функционален. Это когнитивное искажение, известное как «что вы видите, то и есть». Однако в электрохимии химия поверхности — это все.
Прежде чем электрод коснется ячейки, вы должны проверить его целостность:
- Физическая структура: Ищите деформации. Изогнутый электрод изменяет распределение плотности тока.
- Чистота поверхности: Проверьте наличие остатков или коррозии. Пятнышко грязи — это не просто грязь; это катализатор нежелательных побочных реакций.
Если поверхность повреждена, эксперимент обречен еще до его начала. Чистые поверхности — это не роскошь; это предпосылка.
Этап 2: Геометрия выравнивания
После завершения проверки мы переходим к физической установке.
Это игра геометрии. Цель — симметрия и изоляция.
Когда вы опускаете электроды в ячейку, вы пытаетесь создать равномерное электрическое поле. Если электрод установлен криво, поле искажается. Скорости реакции смещаются. Воспроизводимость исчезает.
Правила размещения
- Центральное выравнивание: Медленно регулируйте опорный механизм. Электрод должен быть осью, вокруг которой вращается ячейка.
- Зазор: Убедитесь, что электрод никогда не касается дна или стенок ячейки. Контакт со стеклом может вызвать трещины от напряжения. Контакт с другим электродом вызывает короткое замыкание.
- Зажим: После позиционирования затяните опорные зажимы. Не полагайтесь на гравитацию или трение. Ослабленный электрод вибрирует, а вибрация вносит шум в ваши данные.
Примечание инженера: Дважды проверьте глубину погружения. Погруженная площадь поверхности определяет плотность тока. Если глубина смещается, ваши расчеты нарушаются.
Этап 3: Логика полярности
У химии есть направление.
Подключение источника питания — это не то же самое, что включение тостера. Полярность определяет поток электронов, а следовательно, и ход реакции.
- Анод (+): Здесь происходит окисление.
- Катод (-): Здесь происходит восстановление.
Реверс здесь катастрофичен. Он не просто останавливает эксперимент; он часто разрушает электроды, заставляя окисляться материал, предназначенный для восстановления.
Всегда прослеживайте провод от источника к ячейке. Красный к аноду. Черный к катоду. Не полагайтесь на память. Доверяйте проводу.
Этап 4: Борьба с энтропией (Обслуживание)
Эксперимент не заканчивается, когда питание отключено.
Энтропия — враг лабораторного оборудования. Если оставить электрод влажным от электролита, коррозия начинается немедленно. Соли кристаллизуются. Металл деградирует.
Чтобы сохранить «романтику» точных приборов, вы должны их чистить.
- Немедленная промывка: Сразу удаляйте продукты реакции.
- Химическая ванна: Для благородных металлов, таких как платина, замачивание в разбавленной кислоте (например, 1М азотной кислоте) восстанавливает поверхность.
- Сухое хранение: Влага — медленный убийца. Храните компоненты в сухой среде.
Если вы храните ячейку длительное время, разберите ее. Оставление электролита в герметичной ячейке — приглашение к деградации.
Сводный контрольный список
Профессионал относится к этому процессу как к системе, а не как к рутине.
| Этап | Критическое действие | «Почему» |
|---|---|---|
| Проверка | Проверить на износ и грязь. | Примеси вызывают побочные реакции. |
| Установка | Центрировать и надежно закрепить. | Позиционирование определяет однородность поля. |
| Подключение | Проверить анод (+) / катод (-). | Обратная полярность разрушает электроды. |
| Обслуживание | Чистить, сушить и разбирать. | Коррозия препятствует воспроизводимости. |
Роль надежного оборудования
Процесс имеет первостепенное значение, но оборудование — это фундамент.
Вы не можете выполнять точную работу с неустойчивыми зажимами или нечистыми металлами. Лучший протокол в мире не может компенсировать электрод, который непредсказуемо деградирует, или ячейку, которая деформируется под тепловой нагрузкой.
Вот где на сцену выходит KINTEK.
Мы специализируемся на физической инфраструктуре лаборатории. Наши электролитические ячейки и платиновые или графитовые электроды разработаны для выдерживания жестких условий многократного использования. Мы создаем наше оборудование с жесткими допусками, которые ценят инженеры, гарантируя, что когда вы центрируете электрод, он остается центрированным.
Ваши исследования заслуживают оборудования, которое так же дисциплинировано, как и вы.
Готовы обновить свою электрохимическую установку?
Свяжитесь с нашими экспертами, чтобы обсудить, как KINTEK может поддержать точность вашей лаборатории.
Визуальное руководство
Связанные товары
- Каломельный, хлорсеребряный, сульфатно-ртутный электрод сравнения для лабораторного использования
- Электрод из металлического диска Электрохимический электрод
- Вращающийся дисковый (кольцевой) электрод RRDE / совместим с PINE, японским ALS, швейцарским Metrohm, стеклоуглеродным платиновым
- Вращающийся платиновый дисковый электрод для электрохимических применений
- Платиновая листовая электродная пластина для лабораторных применений в области аккумуляторов
Связанные статьи
- Исчерпывающее руководство по референтным электродам: Типы, области применения и критерии выбора
- Как правильно выбрать электрод сравнения для вашего приложения
- Основы электрохимии:Условия и меры предосторожности при использовании различных эталонных электродов
- Общие эталонные электроды для электрохимических исследований
- Руководство для начинающих по изучению электродов сравнения в электрохимии




















