Требования к использованию эталонных электродов
Идеальный неполяризованный электрод
Идеальный неполяризованный электрод служит краеугольным камнем в электрохимических измерениях, обеспечивая стабильную и надежную точку отсчета. Этот тип электродов характеризуется превосходной обратимостью, благодаря которой потенциал электрода остается неизменным независимо от направления протекания тока. Стабильный потенциал крайне важен, поскольку он сводит к минимуму колебания и ошибки в измерениях, повышая тем самым точность и надежность полученных данных.
Кроме того, воспроизводимость потенциала идеального неполяризованного электрода имеет первостепенное значение. Это означает, что электрод должен стабильно создавать одинаковый потенциал в идентичных условиях, исключая расхождения при повторных экспериментах. Такая воспроизводимость важна для научной строгости и обеспечения надежного сравнения и воспроизведения экспериментальных результатов.
Чтобы проиллюстрировать эти качества, рассмотрим следующую таблицу, в которой сравниваются характеристики идеальных и неидеальных эталонных электродов:
| Характеристика | Идеальный эталонный электрод | Неидеальный эталонный электрод |
|---|---|---|
| Обратимость электрода | Высокая | Низкая |
| Стабильность потенциала | Высокая | Переменная |
| Потенциальная воспроизводимость | Высокий | Низкая |
Таким образом, идеальный неполяризованный электрод должен обладать высокой обратимостью электрода, стабильностью потенциала и отличной воспроизводимостью потенциала, чтобы эффективно работать в качестве эталона в электрохимических исследованиях.
Температурный коэффициент и обслуживание
Температурный коэффициент электрода сравнения - это критический параметр, влияющий на его производительность и надежность. В идеале электрод должен обладать минимальным температурным коэффициентом, обеспечивающим стабильность его потенциала в различных условиях окружающей среды. Такая стабильность крайне важна для точных измерений в электрохимических экспериментах, где даже незначительные колебания потенциала могут привести к существенным ошибкам.
Помимо малого температурного коэффициента, электрод должен быть удобен в изготовлении, эксплуатации и обслуживании. Простота изготовления обеспечивает стабильное качество и доступность, а простота использования упрощает экспериментальную установку и снижает вероятность ошибок при работе. Требования к обслуживанию должны быть минимальными, что позволяет использовать электрод в течение длительного времени без частой калибровки или замены.
| Аспект | Идеальные характеристики | Важность |
|---|---|---|
| Температурный коэффициент | Малый | Обеспечивает стабильность потенциала при различных температурах |
| Изготовление | Легко производить | Обеспечивает стабильное качество и доступность |
| Использование | Простота и интуитивность | Упрощает экспериментальную установку и снижает количество ошибок |
| Техническое обслуживание | Минимальный | Обеспечивает длительное использование без частого вмешательства |
Уделяя внимание этим аспектам, исследователи могут выбирать и обслуживать эталонные электроды, которые обеспечивают надежные и точные данные, способствуя успеху электрохимических исследований.
Условия использования различных эталонных электродов
Классификация на основе pH
При выборе электрода сравнения для электрохимических экспериментов важнейшим фактором является рН электролита. Различные эталонные электроды специально разработаны для оптимального функционирования в различных условиях pH, обеспечивая точность и стабильность измерений.
Кислотные условия
Для сред с низким уровнем pH, каломельные электроды обычно используются каломельные электроды. Эти электроды надежны в кислых условиях благодаря своей стабильности и тому, что они не вступают в реакцию с кислыми растворами. Каломельный электрод состоит из ртути, контактирующей с пастой из хлорида ртути (I) (каломель) и раствора хлорида калия, что обеспечивает стабильный потенциал.

Нейтральные условия
В нейтральных условиях pH, хлорсеребряные электроды являются предпочтительным выбором. Этот тип электродов состоит из серебряной проволоки, покрытой хлоридом серебра, которая погружается в раствор хлорида калия или натрия. Хлоридсеребряный электрод отличается превосходной стабильностью и низким температурным коэффициентом, что делает его пригодным для широкого спектра применений.
Щелочные условия
Для сред с высоким уровнем pH, ртутно-ртутные оксидные электроды используются. Эти электроды изготавливаются из ртути, контактирующей с пастой из оксида ртути и раствора гидроксида калия. Ртутно-ртутно-оксидный электрод стабилен в щелочных условиях и обеспечивает постоянный потенциал, что очень важно для точных измерений в таких средах.
| Тип электрода | Оптимальный диапазон pH | Компоненты |
|---|---|---|
| Каломельный электрод | Кислотные (низкий pH) | Ртуть, ртуть (I) хлоридная паста, раствор хлорида калия |
| Хлорид-серебряный электрод | Нейтральный (средний pH) | Серебряная проволока, покрытая хлоридом серебра, раствором хлорида калия или хлорида натрия |
| Ртутно-меркуриевый оксидный электрод | Щелочной (высокий pH) | Ртуть, паста из оксида ртути, раствор гидроксида калия. |
Понимание специфических требований к pH для каждого типа электродов сравнения позволяет выбрать наиболее подходящий электрод, повышая тем самым точность и надежность электрохимических измерений.
Особые случаи и органические электролиты
В особых случаях, например, при работе с серной кислотой или растворами сульфатов, используются ртутно-меркуриевые электроды благодаря их совместимости с этими жесткими средами. Эти электроды особенно эффективны для поддержания стабильных потенциалов и обеспечения точности измерений в таких агрессивных условиях.
В области аккумуляторных технологий преобладают электроды на основе гидроксида кадмия. Эти электроды выбирают за их способность выдерживать циклические нагрузки при эксплуатации батарей, обеспечивая надежную работу в течение длительного времени.
Для приложений с органическими электролитами часто выбирают серебряные и ферроценовые электроды. Серебряные электроды ценятся за их стабильность и низкую реакционную способность с органическими соединениями, в то время как ферроценовые электроды обладают уникальными преимуществами с точки зрения их окислительно-восстановительных свойств и совместимости с органическими средами.
| Тип электролита | Предпочтительный электрод | Ключевые преимущества |
|---|---|---|
| Растворы серной кислоты | Сульфат ртути | Совместимость с агрессивными средами, стабильный потенциал |
| Аккумуляторная промышленность | Гидроксид кадмия | Выносливость в циклических операциях с батареями, надежная работа |
| Органические электролиты | Серебро и ферроцен | Стабильность при работе с органическими соединениями, уникальные окислительно-восстановительные свойства |
В этой таблице приведены предпочтительные электроды для различных типов электролитов и указаны их ключевые преимущества в различных областях применения.
Почему разные эталонные электроды применяются в разных условиях
Реакция электрода и уравнение Нернста
Различные электроды подбираются для конкретных условий на основе их уникальных электродных реакций и получаемых в результате стандартных равновесных электродных потенциалов, которые тщательно рассчитываются с помощью уравнения Нернста. Это уравнение, названное в честь немецкого химика Вальтера Нернста, является основополагающим в электрохимии, поскольку оно связывает восстановительный потенциал электрохимической реакции со стандартным электродным потенциалом и активностью реагирующих видов.
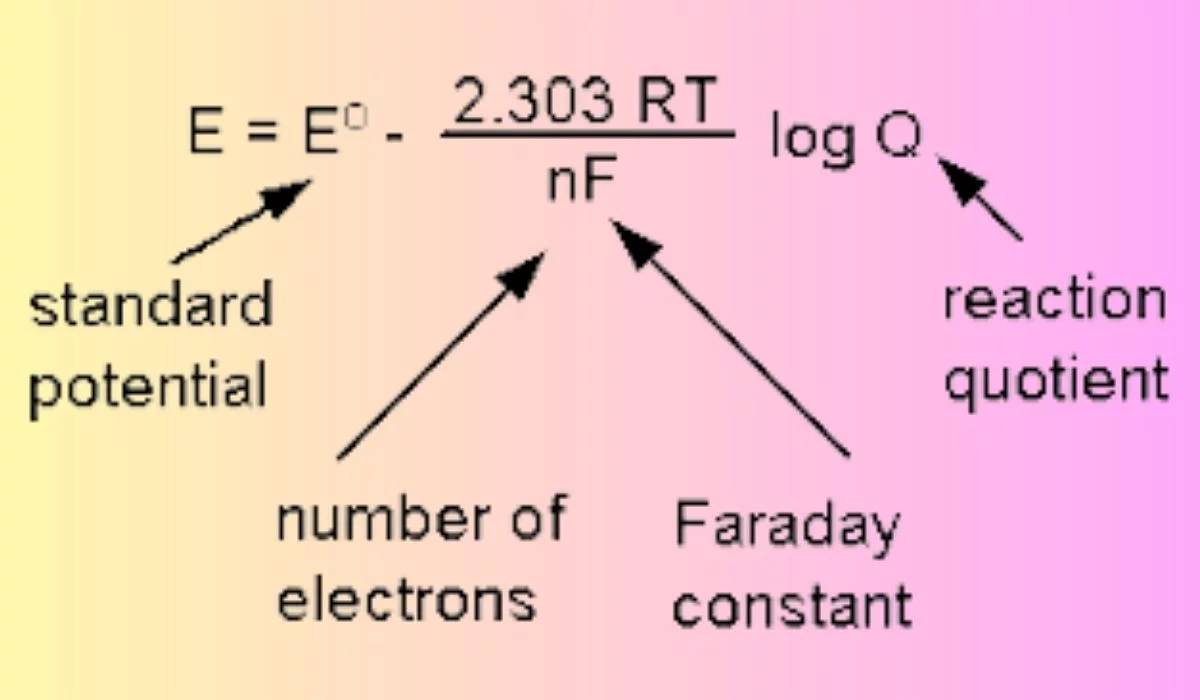
Например, стандартный равновесный электродный потенциал хлоридсеребряного электрода, часто используемого в нейтральных средах, зависит от концентрации хлорид-ионов и парциального давления газообразного водорода. Напротив, каломельный электрод, используемый в кислых условиях, работает по другим термодинамическим принципам, обеспечивая стабильность и точность в заданной среде.
| Тип электрода | Подходящие условия | Ключевая реакция | Стандартный равновесный потенциал (В) |
|---|---|---|---|
| Хлорид серебра | Нейтральный | AgCl + e- → Ag + Cl- | 0.2223 |
| Каломель | Кислотный | Hg₂Cl₂ + 2e- → 2Hg + 2Cl- | 0.2682 |
| Ртуть - оксид ртути | Щелочной | HgO + H₂O + 2e- → Hg + 2OH- | 0.0977 |
Выбор подходящего электрода имеет решающее значение, поскольку он напрямую влияет на точность и надежность электрохимических измерений. Пригодность каждого электрода определяется его способностью поддерживать стабильный потенциал в изменяющихся условиях, что гарантирует, что уравнение Нернста точно предсказывает поведение электрода. Такая точность очень важна для различных приложений - от мониторинга окружающей среды до аккумуляторных технологий, где даже незначительные отклонения могут привести к существенным ошибкам.
Таким образом, уравнение Нернста не только определяет количественную зависимость между потенциалом электрода и условиями реакции, но и подчеркивает важность выбора правильного электрода для конкретных приложений. Это гарантирует, что электрохимические эксперименты дадут точные и воспроизводимые результаты, соответствующие более широким целям научного поиска и промышленной практики.
Стабильность и недостатки
Хлоридсеребряный электрод служит ярким примером того, как конкретные условия могут влиять на стабильность и точность эталонных электродов. В щелочных условиях длительное использование этого электрода может привести к образованию оксида серебра. Эта реакция не только нарушает стабильность электрода, но и снижает его точность, тем самым влияя на достоверность проводимых измерений.
В щелочной среде химическая реакция может быть представлена следующим образом:
- Хлорид серебра (AgCl) + гидроксид (OH-) → оксид серебра (Ag₂O) + хлорид (Cl-).
Это превращение значительно изменяет потенциал электрода, делая его менее предсказуемым и более подверженным ошибкам. Нестабильность, вызванная образованием оксида серебра, требует тщательного подхода при выборе и использовании электродов сравнения в таких условиях.
Для уменьшения этих недостатков часто рекомендуется использовать систему двойного солевого моста. Этот метод помогает поддерживать стабильность хлоридсеребряного электрода в щелочных условиях, обеспечивая более точные и надежные показания.
Устранение недостатков с помощью солевых мостиков
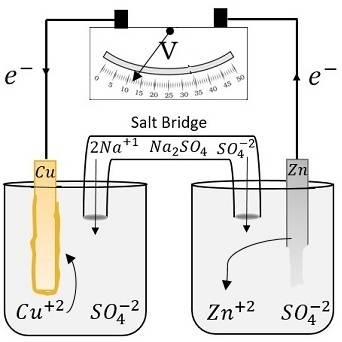
В щелочных условиях хлорсеребряные электроды могут столкнуться с проблемами стабильности из-за образования оксида серебра с течением времени, что влияет на точность и надежность измерений. Для борьбы с этими недостатками эффективной стратегией является использование системы двойного солевого моста.
Система двойного солевого моста предполагает использование двух отдельных солевых мостов, каждый из которых заполнен соответствующим электролитом. Такая система позволяет изолировать электрод сравнения от испытуемого раствора, тем самым снижая риск загрязнения и сводя к минимуму взаимодействие, которое может привести к образованию оксида серебра. Создавая буферную зону, система двойного солевого моста обеспечивает стабильность эталонного электрода даже в сложных щелочных средах.
Этот метод не только сохраняет целостность хлоридсеребряного электрода, но и повышает общую точность электрохимических измерений. Двойная изоляция, обеспечиваемая солевыми мостиками, действует как защитный барьер, позволяя более последовательно и надежно собирать данные в щелочных условиях.
Связанные товары
- Каломельный, хлорсеребряный, сульфатно-ртутный электрод сравнения для лабораторного использования
- Сульфатно-медный электрод сравнения для лабораторного использования
- Электрод из металлического диска Электрохимический электрод
- Графитовый дисковый стержневой и листовой электрод Электрохимический графитовый электрод
- Электрод из стеклоуглерода



















