Графитовые стержни служат катодами в нескольких ключевых электрохимических процессах, в первую очередь в промышленном электролизе солей и в обычных сухих элементах. В этих приложениях основная функция графитового стержня заключается не в потреблении или реакции, а в том, чтобы выступать в качестве химически инертной и электропроводящей поверхности, на которой может происходить реакция восстановления.
Графит выбирают в качестве катодного материала не потому, что он участвует в основной реакции, а потому, что он является превосходным инертным проводником. Его уникальное сочетание электропроводности, химической стойкости, высокой термической стабильности и низкой стоимости делает его идеальной платформой для протекания реакции восстановления.

Почему графит является идеальным катодным материалом
Выбор материала для электрода является критически важным конструктивным решением в любой электрохимической ячейке. Графит (особая форма углерода) обладает набором свойств, которые делают его исключительно подходящим для роли катода.
Отличная электропроводность
Графит имеет уникальную слоистую, плоскую структуру. Внутри этих слоев делокализованные электроны могут свободно перемещаться, что позволяет графиту очень эффективно проводить электричество — необходимое свойство для любого электрода.
Высокая химическая инертность
В качестве катода электрод должен способствовать переносу электронов к веществу в электролите, не вступая в реакцию сам. Углерод относительно неактивен, особенно по сравнению с большинством металлов, что означает, что он не будет корродировать или мешать желаемому химическому процессу.
Термическая стабильность
Графит имеет одну из самых высоких температур плавления/сублимации среди всех элементов (около 3652°C или 6606°F). Это делает его идеальным для высокотемпературных электрохимических процессов, таких как электролиз расплавленных солей, где металлические электроды расплавились бы.
Низкая стоимость и доступность
С промышленной точки зрения графит является обильным и недорогим материалом. Это делает крупномасштабное электрохимическое производство, требующее больших электродов, экономически целесообразным.
Ключевые области применения графитовых катодов
Понимание конкретных сценариев использования проясняет теорию. В каждом примере графитовый катод — это просто место, куда доставляются электроны, вызывающие химическое изменение.
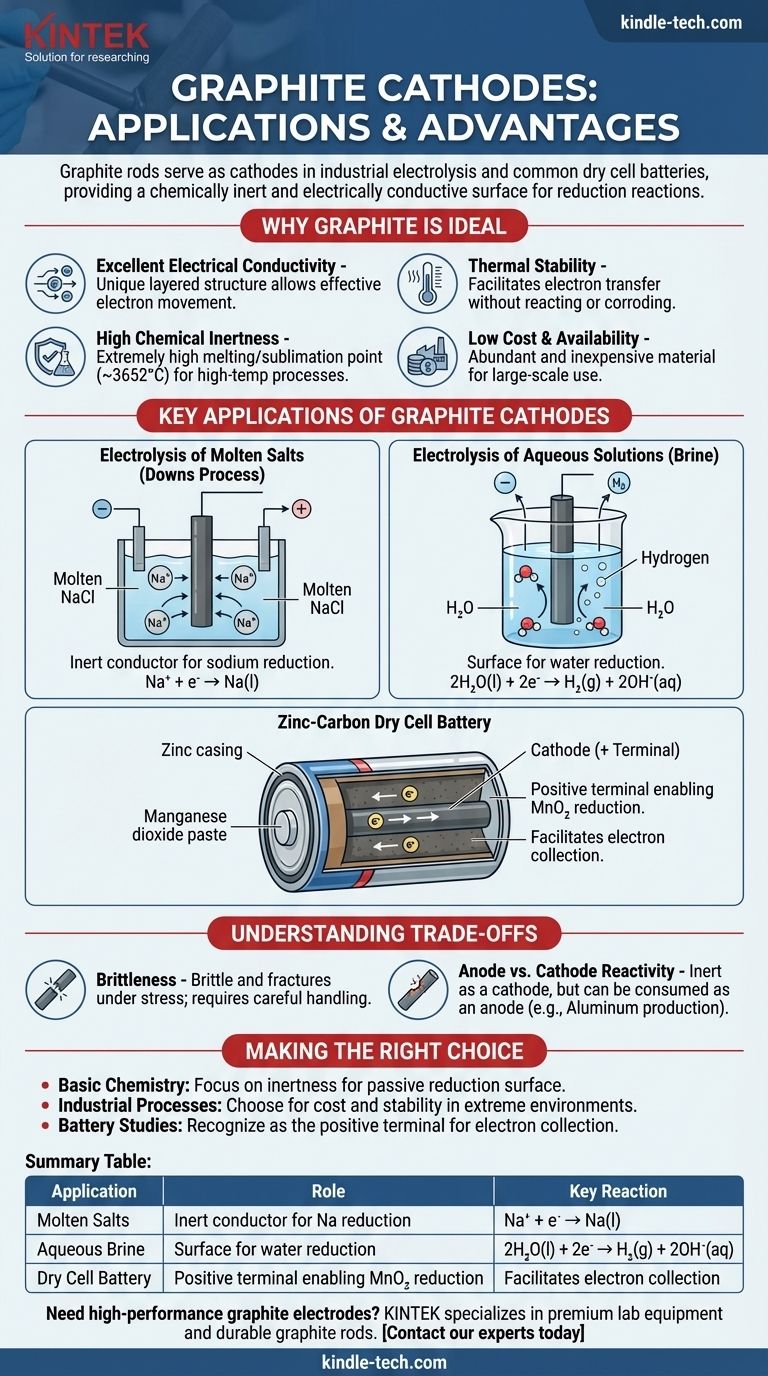
Электролиз расплавленных солей (процесс Даунса)
При производстве чистого металлического натрия из расплавленного хлорида натрия (NaCl) в качестве катода часто используется графитовый стержень. Положительно заряженные ионы натрия (Na⁺) притягиваются к отрицательно заряженному катоду, где они принимают электрон и восстанавливаются до жидкого металлического натрия.
Na⁺ + e⁻ → Na(l)
Графитовый катод просто обеспечивает поверхность и электроны для этой реакции.
Электролиз водных растворов (рассол)
При электролизе водного раствора хлорида натрия (рассола) графитовый катод выполняет аналогичную роль. Однако в этом случае вода легче восстанавливается, чем ионы натрия.
Следовательно, молекулы воды восстанавливаются на поверхности графитового катода с образованием газообразного водорода и гидроксид-ионов.
2H₂O(l) + 2e⁻ → H₂(g) + 2OH⁻(aq)
Цинк-углеродный сухой элемент
В распространенном «тяжелом» аккумуляторе центральный стержень изготовлен из графита и действует как катод (положительный полюс). Он окружен влажной пастой из диоксида марганца (MnO₂) и других химических веществ.
Графитовый стержень собирает электроны из внешней цепи. Реакция восстановления происходит в пасте рядом со стержнем, где диоксид марганца восстанавливается. Графит просто облегчает этот процесс.
Понимание компромиссов
Хотя графит высокоэффективен, он не является идеальным материалом. Понимание его ограничений является ключом к пониманию его применения.
Хрупкость
В отличие от металлов, которые являются пластичными, графит хрупок и может разрушиться при механическом ударе или напряжении. Это требует осторожного обращения и поддержки в промышленных конструкциях.
Реакционная способность анода и катода
Хотя графит очень инертен в качестве катода, он может расходоваться при использовании в качестве анода (места окисления) в некоторых процессах. Например, при производстве алюминия анод из углерода реагирует с выделяющимся кислородом с образованием газообразного CO₂ и постепенно сгорает.
Путаница между типами ячеек
Распространенный источник путаницы — полярность электрода. Катод всегда является местом восстановления, но его знак меняется в зависимости от типа ячейки.
- В электролитической ячейке (например, для электролиза солей) катод является отрицательным полюсом.
- В гальванической ячейке (например, в аккумуляторе) катод является положительным полюсом.
Сделайте правильный выбор для вашей цели
Причина, по которой вы спрашиваете о графитовых катодах, определяет, на каком аспекте наиболее важно сосредоточиться.
- Если ваше основное внимание уделяется базовой химии: Помните, что графит — это инертный проводник, обеспечивающий пассивную поверхность для протекания реакции восстановления без участия в ней.
- Если ваше основное внимание уделяется промышленным процессам: Выбирайте графит за его экономическую эффективность и непревзойденную стабильность в высокотемпературных или агрессивных средах, где большинство металлов вышли бы из строя.
- Если ваше основное внимание уделяется изучению аккумуляторов: Признайте, что графитовый стержень в цинк-углеродном элементе действует как положительный полюс (катод), служащий коллектором электронов, который обеспечивает восстановление окружающего химического пастообразного вещества.
В конечном счете, понимание роли графита в качестве катода заключается в признании силы инертного, проводящего материала, который обеспечивает химию, не вмешиваясь в нее.
Сводная таблица:
| Применение | Роль графитового катода | Ключевая реакция |
|---|---|---|
| Электролиз расплавленных солей (процесс Даунса) | Инертный проводник для восстановления натрия | Na⁺ + e⁻ → Na(l) |
| Электролиз водного рассола | Поверхность для восстановления воды | 2H₂O(l) + 2e⁻ → H₂(g) + 2OH⁻(aq) |
| Цинк-углеродный сухой элемент | Положительный полюс, обеспечивающий восстановление MnO₂ | Облегчает сбор электронов |
Нужны высокоэффективные графитовые электроды для ваших электрохимических процессов? KINTEK специализируется на премиальном лабораторном оборудовании и расходных материалах, включая прочные графитовые стержни, разработанные для превосходной проводимости и термической стабильности. Независимо от того, проводите ли вы промышленный электролиз или разрабатываете аккумуляторные технологии, наши материалы обеспечивают надежную инертную работу. Свяжитесь с нашими экспертами сегодня, чтобы найти идеальное графитовое решение для ваших лабораторных нужд!
Визуальное руководство
Связанные товары
- Графитовый дисковый стержневой и листовой электрод Электрохимический графитовый электрод
- Углеграфитовая пластина, изготовленная методом изостатического прессования
- Графитовый тигель высокой чистоты для испарения
- Высокочистый графитовый тигель для электронно-лучевого испарения
- Графитовый лодочный тигель для лабораторной трубчатой печи с крышкой
Люди также спрашивают
- Какова правильная процедура установки и подключения графитового электрода во время эксперимента? Обеспечьте точные электрохимические результаты
- Как следует предварительно обрабатывать графитовый электрод перед использованием? Обеспечение надежных электрохимических данных
- Почему для электролитического получения индия предпочтительны размерно-стабильные аноды (DSA)? Обеспечение высокочистых результатов.
- Какова типичная роль графитового электрода в электрохимической установке? Эффективно завершите свою цепь
- Какой путь реакции и механизм связаны с использованием графитовых электродов при переработке биомассы?






