С технической точки зрения, электролитическая ячейка — это особый тип электрохимической ячейки. Хотя она и относится к этой широкой категории, важно понимать, что «электрохимическая ячейка» также описывает другое устройство — гальваническую ячейку, — которое выполняет прямо противоположную функцию.
Ключевое различие заключается в следующем: электролитическая ячейка использует внешнюю электрическую энергию для принудительного протекания химической реакции, которая не произошла бы сама по себе. Она потребляет энергию. В отличие от нее, гальваническая ячейка (например, батарея) использует самопроизвольную химическую реакцию для выработки электрической энергии.

Основная функция: Принуждение к химической реакции
Что такое электролиз?
Электролиз — это процесс использования постоянного электрического тока (DC) для запуска несамопроизвольной химической реакции. Проще говоря, это использование электричества для осуществления химического изменения.
Устройство, в котором происходит этот процесс, называется электролитической ячейкой или электролизером.
Роль внешнего источника питания
Определяющей особенностью электролитической ячейки является ее потребность во внешнем источнике питания, таком как батарея или блок питания. Это внешнее напряжение преодолевает естественный энергетический барьер реакции, заставляя химические вещества реагировать.
Ключевые компоненты
Электролитическая ячейка состоит из двух электродов, анода и катода, погруженных в жидкий раствор, называемый электролитом. Внешний источник питания отводит электроны от анода (окисление) и подает их на катод (восстановление), вызывая желаемое химическое изменение.
Электролитическая против гальванической: зонтик «Электрохимическая ячейка»
Термин электрохимическая ячейка является родительской категорией для любого устройства, которое преобразует химическую и электрическую энергию. Понимание двух основных типов важно для ясности.
Электролитические ячейки: Потребители энергии
Эти ячейки потребляют электрическую энергию для осуществления химического изменения. Их основная цель — создание веществ или изменение материалов посредством принудительной реакции.
Распространенным примером является использование электролитической ячейки для расщепления воды (H₂O) на водород и кислород — процесс, требующий значительных затрат энергии.
Гальванические (Вольтовы) ячейки: Производители энергии
Эти ячейки делают наоборот. Они используют самопроизвольную химическую реакцию для выработки электрического тока. Это фундаментальный принцип, лежащий в основе всех обычных батарей.
Когда вы используете батарею, вы используете гальваническую ячейку для преобразования запасенной химической энергии в полезную электрическую мощность.
Почему это различие имеет значение
Называть электролитическую ячейку «электрохимической ячейкой» технически правильно, но неточно. Это все равно что называть квадрат «прямоугольником». Хотя это правда, это упускает из виду специфические свойства, которые его определяют. Ключевое различие всегда заключается в направлении преобразования энергии.
Общие области применения и компромиссы
Где используется электролиз
Способность принудительно проводить химические реакции имеет огромное промышленное значение. Электролитические ячейки необходимы для получения чистого водорода в качестве топлива, выплавки таких металлов, как алюминий и медь, из руды, а также для гальванического нанесения на изделия тонкого слоя металла, такого как хром или золото.
Основной компромисс: Энергозатраты
Основным ограничением электролиза является высокое энергопотребление. Поскольку вы заставляете протекать несамопроизвольную реакцию, этот процесс всегда требует больше энергии, чем химическая энергия, которую вы запасаете, или ценность создаваемого вами продукта. Эти затраты энергии являются центральным экономическим и экологическим соображением для любого промышленного процесса электролиза.
Как выбрать подходящую ячейку для вашей цели
- Если ваша основная цель — хранение энергии или создание материалов (например, водородного топлива или чистого алюминия): вы имеете дело с электролитической ячейкой, которая потребляет электричество для проведения химической реакции.
- Если ваша основная цель — выработка энергии из химического источника (например, батарея): вы имеете дело с гальванической (или вольтовой) ячейкой, которая производит электричество в результате самопроизвольной реакции.
- Если ваша основная цель — общая научная область, охватывающая оба процесса: следует использовать общее название электрохимическая ячейка.
В конечном счете, понимание направления потока энергии — потребляется она или производится — является ключом к различению этих фундаментальных устройств.
Сводная таблица:
| Характеристика | Электролитическая ячейка | Гальваническая ячейка |
|---|---|---|
| Преобразование энергии | Потребляет электрическую энергию | Вырабатывает электрическую энергию |
| Тип реакции | Несамопроизвольная (принудительная) | Самопроизвольная |
| Основная функция | Создание веществ (например, H₂, очищенные металлы) | Выработка энергии (например, батареи) |
| Источник питания | Требует внешнего источника (например, батареи, блока питания) | Сама является источником питания |
Нужен точный контроль химических реакций в вашей лаборатории?
Независимо от того, связаны ли ваши исследования с синтезом материалов, гальваническим покрытием или накоплением энергии, наличие правильного оборудования имеет решающее значение. KINTEK специализируется на высококачественном лабораторном оборудовании и расходных материалах, включая электрохимические ячейки и блоки питания, разработанные для надежности и точности.
Позвольте нашим экспертам помочь вам выбрать идеальную установку для вашего конкретного применения. Свяжитесь с нашей командой сегодня, чтобы обсудить ваши лабораторные потребности и узнать, как KINTEK может поддержать ваши исследовательские цели.
Визуальное руководство
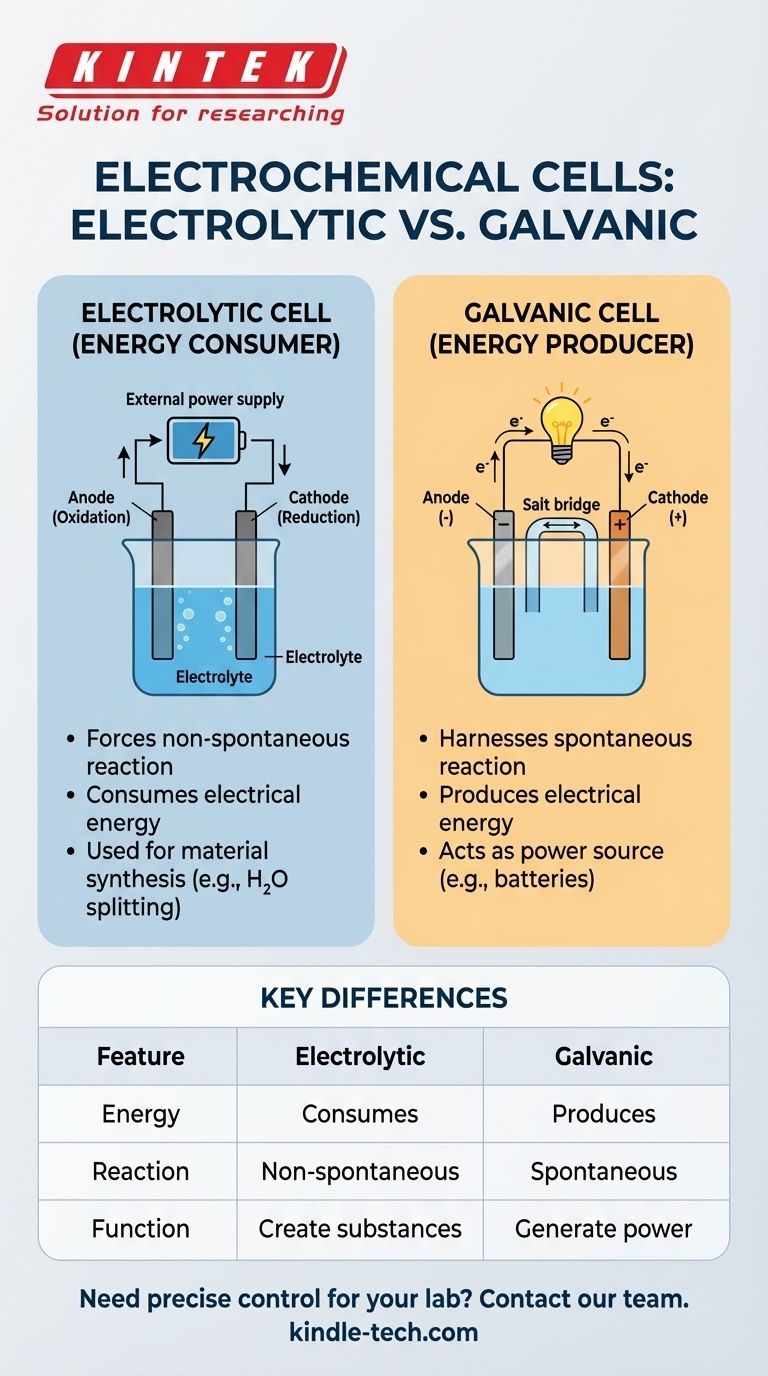
Связанные товары
- Настраиваемые электролизеры PEM для различных исследовательских применений
- Электрохимическая ячейка для спектроэлектролиза в тонком слое
- Электрохимическая ячейка с газодиффузионным электролизом и ячейка для реакции с протоком жидкости
- Кварцевая электрохимическая ячейка для электрохимических экспериментов
- Электрохимическая ячейка из ПТФЭ, коррозионностойкая, герметичная и негерметичная
Люди также спрашивают
- Каковы конфигурации отверстий для незапечатанной и запечатанной версий электролитической ячейки? Оптимизируйте вашу электрохимическую установку
- Какова немедленная процедура очистки электролизной ячейки после использования? Предотвратите накопление отложений для получения точных результатов
- Каковы меры предосторожности при нагревании или стерилизации электролитической ячейки? Избегайте повреждения чувствительных компонентов
- Какие параметры должны строго контролироваться в процессе электролиза? Обеспечьте точность и эффективность
- Какова надлежащая процедура хранения электролитической ячейки и ее компонентов? Пошаговое руководство по сохранению точности



















