Термин «электрод» не является единой категорией. Вместо этого электроды классифицируются несколькими различными способами в зависимости от их роли в реакции, их химического участия и их функции в измерительной системе. Понимание этих различных систем классификации является ключом к осмыслению их назначения в любой электрохимической ячейке.
Самое важное понимание заключается в том, что «тип» электрода определяется его контекстом. Один и тот же кусок металла может быть анодом или катодом, активным или инертным, в зависимости от электрохимической системы, в которую вы его помещаете.
Классификация 1: По электрохимической роли
Наиболее фундаментальная классификация определяет электрод по его роли в двух половинах электрохимической реакции: окислении и восстановлении.
Анод: Место окисления
Анод, по определению, — это электрод, на котором происходит окисление — потеря электронов. Вещества на аноде отдают свои электроны электроду.
Катод: Место восстановления
Катод — это электрод, на котором происходит восстановление — приобретение электронов. Катод отдает свои электроны веществам в растворе.
Ключевое различие: Полярность анода/катода
Распространенным источником путаницы является заряд (+ или -) анода и катода. Эта полярность зависит от типа ячейки:
- В гальваническом элементе (например, в батарее) самопроизвольная реакция генерирует энергию. Анод является отрицательным полюсом, а катод — положительным полюсом.
- В электролитической ячейке внешний источник питания вызывает несамопроизвольную реакцию. Анод является положительным полюсом, а катод — отрицательным полюсом.
Классификация 2: По химическому участию
Эта классификация описывает, участвует ли сам материал электрода в химической реакции.
Активные электроды: Участники реакции
Активный электрод изготовлен из материала, который либо расходуется, либо образуется в ходе реакции ячейки. Например, в цинково-медном аккумуляторе цинковый анод растворяется, активно участвуя в реакции окисления.
Инертные электроды: Поверхность для реакции
Инертный электрод не участвует в химической реакции. Он служит только в качестве проводящей поверхности, на которой может происходить окисление или восстановление. Платина и углерод (графит) являются распространенными инертными электродами, используемыми для облегчения реакций с участием газов или растворенных ионов.
Классификация 3: По измерительной функции
В аналитической электрохимии для точных измерений часто используется трехэлектродная система. Это приводит к функциональной классификации.
Рабочий электрод
Это электрод, на котором происходит интересующая реакция. Его потенциал является основной контролируемой или измеряемой переменной.
Электрод сравнения: Стабильный эталон
Электрод сравнения обеспечивает стабильный, постоянный потенциал, относительно которого измеряется потенциал рабочего электрода. Его собственный потенциал не меняется независимо от протекающего тока или состава основного раствора.
Вспомогательный (или противодействующий) электрод
Единственная цель этого электрода — замкнуть электрическую цепь. Он пропускает весь ток, необходимый рабочему электроду, гарантируя, что через чувствительный электрод сравнения протекает незначительный ток, тем самым сохраняя его стабильность.
Понимание компромиссов: Распространенные электроды сравнения
Выбор электрода сравнения имеет решающее значение для точных измерений и зависит от химической среды.
Ag/AgCl: Общая рабочая лошадка
Электрод серебро/хлорид серебра (Ag/AgCl) является наиболее распространенным электродом сравнения. Он стабилен, недорог и, как правило, надежен, что делает его выбором по умолчанию для многих водных растворов.
Насыщенный каломельный электрод (НКЭ): Классическая альтернатива
Насыщенный каломельный электрод (НКЭ) является более старым, высокостабильным стандартом. Он часто используется в ситуациях, когда анализируемый раствор несовместим с ионами серебра или хлорида, которые могут мешать работе электрода Ag/AgCl.
Проблема ртути: Ключевое ограничение
Основным недостатком НКЭ является то, что он содержит ртуть. Это делает его непригодным для применения в пищевых продуктах, напитках или экологических испытаниях, где загрязнение ртутью является серьезной проблемой.
Сделайте правильный выбор для вашей цели
Ваше применение определяет, какая классификация наиболее важна.
- Если ваше основное внимание уделяется пониманию основной химии батарей: Освойте концепции анода/катода и активных/инертных электродов.
- Если ваше основное внимание уделяется проведению электрохимического анализа (например, вольтамперометрии): Трехэлектродная система (рабочий, сравнения, вспомогательный) является необходимой основой.
- Если ваше основное внимание уделяется выбору датчика для конкретной среды: Ваша главная забота будет заключаться в химической совместимости и стабильности вашего электрода сравнения, например, выборе между Ag/AgCl и альтернативой.
Понимание этих перекрывающихся классификаций дает вам возможность контролировать и интерпретировать поведение любой электрохимической системы.

Сводная таблица:
| Классификация | Ключевые типы | Основная функция |
|---|---|---|
| Электрохимическая роль | Анод, Катод | Определяют места окисления/восстановления; полярность зависит от типа ячейки (гальваническая/электролитическая) |
| Химическое участие | Активный, Инертный | Указывает, участвует ли материал электрода в реакции или служит только поверхностью |
| Измерительная функция | Рабочий, Сравнения, Вспомогательный | Обеспечивают точный контроль и измерение в аналитической электрохимии |
Нужна помощь в выборе правильных электродов для электрохимических применений в вашей лаборатории? В KINTEK мы специализируемся на предоставлении высококачественного лабораторного оборудования и расходных материалов, адаптированных к вашим исследовательским потребностям. Независимо от того, занимаетесь ли вы разработкой батарей, проектированием датчиков или аналитическими измерениями, наш опыт гарантирует, что вы получите оптимальные электроды для точности и производительности. Свяжитесь с нами сегодня, чтобы обсудить ваши требования и улучшить ваши электрохимические рабочие процессы!
Визуальное руководство
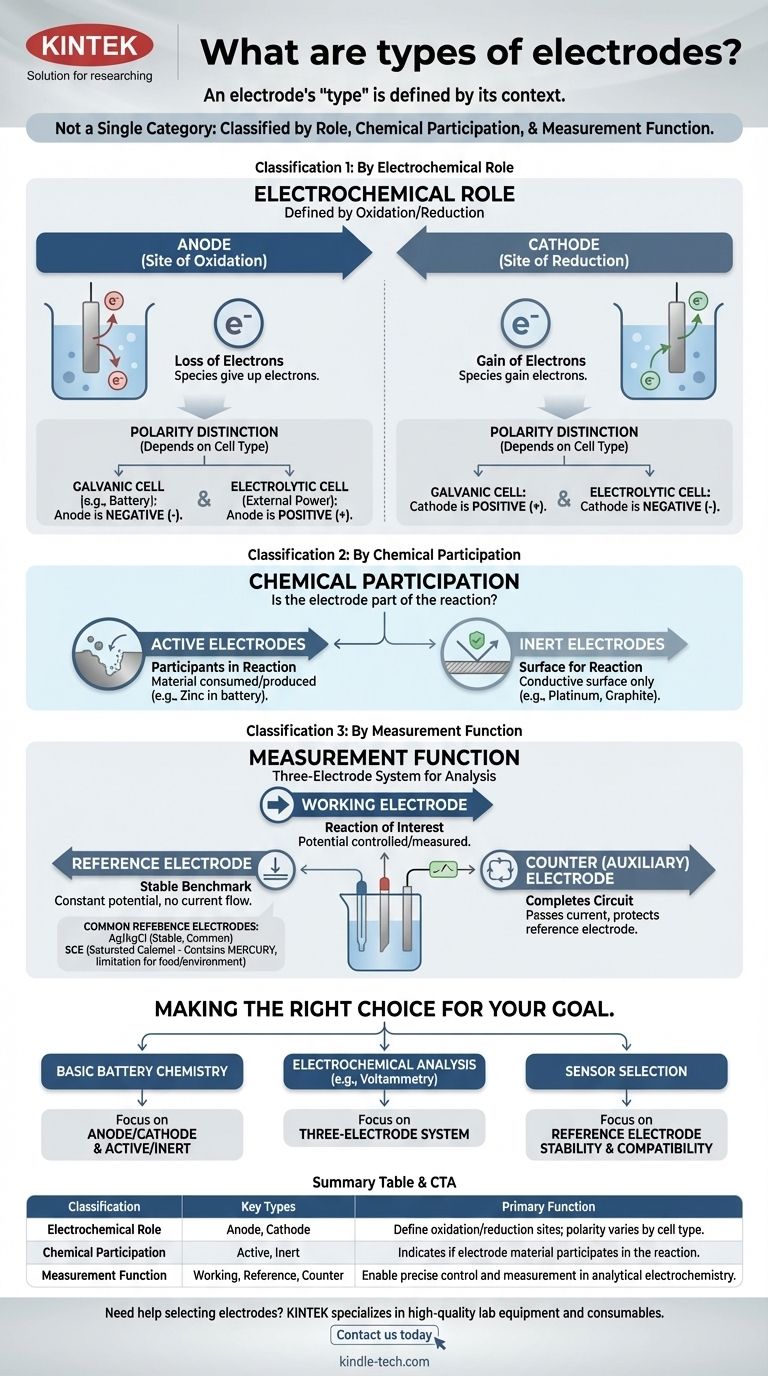
Связанные товары
- Каломельный, хлорсеребряный, сульфатно-ртутный электрод сравнения для лабораторного использования
- Электрод из металлического диска Электрохимический электрод
- Вращающийся дисковый (кольцевой) электрод RRDE / совместим с PINE, японским ALS, швейцарским Metrohm, стеклоуглеродным платиновым
- Вращающийся платиновый дисковый электрод для электрохимических применений
- Платиновая листовая электродная пластина для лабораторных применений в области аккумуляторов
Люди также спрашивают
- Какова цель референсного электрода? Достижение стабильных и точных электрохимических измерений
- Что такое электрод сравнения в потенциометрии? Ключ к стабильным и точным измерениям
- Какой тип электрода можно использовать в качестве точки отсчета? Выберите правильный для точных измерений
- Какова функция электрода сравнения? Освойте точность при реконструкции трехэлектродных реакторов
- Какой электрод используется в качестве заземляющего электрода сравнения? Освойте ключ к точным электрохимическим измерениям



















