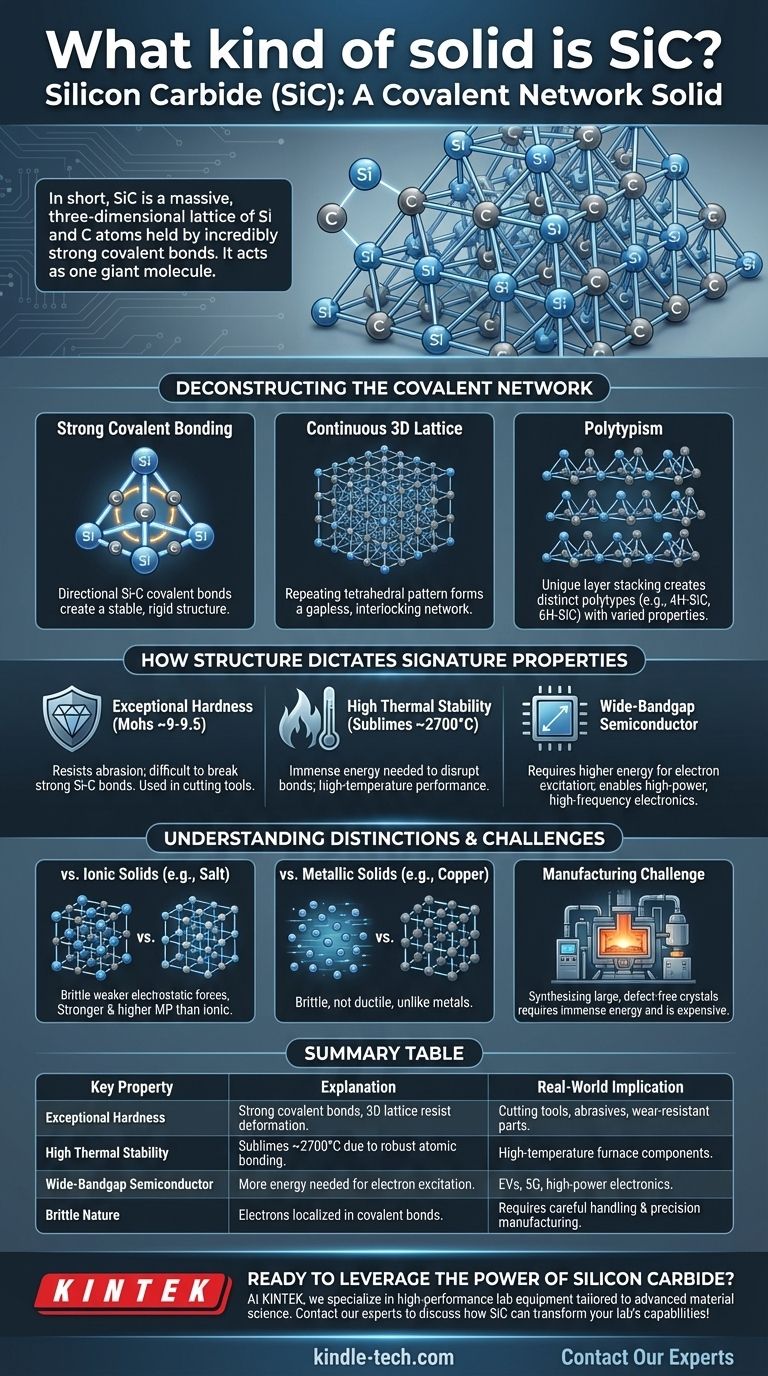
Коротко говоря, карбид кремния (SiC) — это ковалентное сетевое твердое тело. Эта классификация означает, что его атомы кремния и углерода связаны в массивную трехмерную решетку, удерживаемую чрезвычайно прочными и направленными ковалентными связями. В отличие от молекулярных твердых тел со слабыми силами между молекулами, весь кристалл SiC фактически действует как одна гигантская молекула.
Классификация SiC как ковалентного сетевого твердого тела — это не просто ярлык; это фундаментальное объяснение его исключительных свойств. Понимание его жесткой атомной решетки является ключом к постижению его чрезвычайной твердости, высокотемпературной стабильности и уникального электронного поведения.

Деконструкция ковалентной сетевой структуры
Чтобы понять SiC, вы должны сначала представить его базовую атомную архитектуру. Именно эта структура определяет почти все его полезные характеристики.
Природа ковалентной связи в SiC
Карбид кремния образуется из атомов кремния (Si) и углерода (C). Эти два элемента имеют относительно небольшую разницу в электроотрицательности, что приводит к тому, что они делят электроны и образуют очень прочные, стабильные ковалентные связи.
Эти связи очень направлены. Каждый атом углерода связан с четырьмя атомами кремния, и каждый атом кремния связан с четырьмя атомами углерода в жесткой тетраэдрической конфигурации.
Непрерывная 3D-решетка
Этот тетраэдрический тип связи бесконечно повторяется во всех трех измерениях. Это создает непрерывную, взаимосвязанную сеть без слабых мест или отдельных молекул.
Представьте себе структуру, похожую на алмаз, но с чередующимися атомами кремния и углерода вместо только углерода. Эта жесткая, бесщелевая структура является источником огромной физической прочности SiC.
Концепция политипизма
Уникальной особенностью SiC является политипизм. Хотя локальная тетраэдрическая связь Si-C постоянна, слои этих тетраэдров могут быть расположены в различных последовательностях.
Эти различные способы укладки создают отдельные кристаллические структуры, называемые политипами, такие как 4H-SiC и 6H-SiC. Хотя все они являются SiC, эти политипы имеют немного разные электронные свойства, что делает их подходящими для различных полупроводниковых применений.
Как структура определяет характерные свойства SiC
Модель ковалентной сети напрямую объясняет, почему SiC ведет себя именно так. Макроскопические свойства материала являются прямым следствием его микроскопической связи и структуры.
Исключительная твердость и прочность
Чтобы поцарапать или деформировать SiC, необходимо физически разорвать мощные ковалентные связи Si-C. Поскольку весь кристалл представляет собой единую сеть этих связей, он проявляет невероятную устойчивость к истиранию и деформации.
По шкале Мооса твердость SiC (~9-9,5) уступает только алмазу (10), что делает его элитным материалом для режущих инструментов, абразивов и износостойких компонентов.
Высокая термическая стабильность
Плавление или разрушение твердого тела требует придания его атомам достаточной энергии для преодоления сил, удерживающих их вместе. Огромная прочность ковалентных связей Si-C означает, что для разрушения решетки требуется огромное количество тепловой энергии.
Следовательно, SiC не плавится при атмосферном давлении, а сублимирует (превращается непосредственно в газ) при чрезвычайно высоких температурах, около 2700 °C (4900 °F).
Уникальное полупроводниковое поведение
Хотя прочные связи характерны для электрического изолятора, такого как алмаз, энергия, необходимая для возбуждения электрона в проводящее состояние (ширина запрещенной зоны) в SiC меньше, чем в алмазе.
Это помещает SiC в особую категорию широкозонных полупроводников. Его запрещенная зона значительно шире, чем у чистого кремния, что позволяет электронике на основе SiC работать при гораздо более высоких напряжениях, температурах и частотах.
Понимание компромиссов и различий
Размещение SiC в контексте других твердых тел проясняет его уникальное положение. Его свойства являются компромиссом, определяемым его связями.
SiC против ионных твердых тел (например, соли)
Ионные твердые тела, такие как хлорид натрия (NaCl), удерживаются ненаправленным электростатическим притяжением между положительными и отрицательными ионами. Хотя они образуют кристаллы, эти связи обычно слабее, чем ковалентные связи SiC, что делает их мягче и значительно снижает их температуры плавления.
SiC против металлических твердых тел (например, меди)
Металлы характеризуются "морем" делокализованных электронов, окружающих решетку положительных ионов. Это электронное море позволяет металлам быть проводящими и пластичными (ковкими). Напротив, электроны SiC заперты в локализованных ковалентных связях, что делает его полупроводником и по своей природе хрупким.
Проблема производства
Сама прочность, которая делает SiC таким желанным, также делает его невероятно трудным в производстве. Синтез больших, бездефектных монокристаллов SiC требует огромной энергии и сложных процессов (таких как метод Лели), что делает его значительно дороже кремния.
Правильный выбор для вашего применения
Понимание классификации SiC как ковалентного сетевого твердого тела позволяет предсказывать его поведение и наилучшие варианты использования.
- Если ваше основное внимание уделяется механическим характеристикам: Признайте, что его ковалентная сеть является прямым источником его высочайшей твердости и износостойкости, что делает его идеальным для абразивов, пескоструйной обработки и прочных механических уплотнений.
- Если ваше основное внимание уделяется силовой электронике: Поймите, что его ковалентная сеть создает широкозонный полупроводник, необходимый для создания надежных силовых инверторов, зарядных устройств для электромобилей и модулей связи 5G, превосходящих кремний.
- Если ваше основное внимание уделяется материаловедению: Классифицируйте SiC как прототип ковалентного сетевого твердого тела, используя его в качестве эталона твердости и термической стабильности при сравнении с другими передовыми керамиками, такими как нитрид бора или нитрид кремния.
В конечном итоге, знание того, что карбид кремния является ковалентным сетевым твердым телом, является первым принципом в понимании и применении его выдающихся возможностей.
Сводная таблица:
| Ключевое свойство | Объяснение | Практическое применение |
|---|---|---|
| Исключительная твердость | Прочные ковалентные связи в 3D-решетке сопротивляются деформации. | Идеально подходит для режущих инструментов, абразивов и износостойких деталей. |
| Высокая термическая стабильность | Сублимирует при ~2700°C благодаря прочным атомным связям. | Подходит для высокотемпературных применений, таких как компоненты печей. |
| Широкозонный полупроводник | Электронам требуется больше энергии для возбуждения, что обеспечивает работу при высокой мощности. | Используется в электромобилях, технологиях 5G и силовой электронике для превосходной производительности. |
| Хрупкость | Электроны локализованы в ковалентных связях, что ограничивает пластичность. | Требует осторожного обращения и точных производственных процессов. |
Готовы использовать мощь карбида кремния в своей лаборатории? В KINTEK мы специализируемся на предоставлении высокопроизводительного лабораторного оборудования и расходных материалов, адаптированных к потребностям передового материаловедения. Независимо от того, разрабатываете ли вы полупроводники нового поколения или вам нужны прочные компоненты для высокотемпературных процессов, наш опыт гарантирует, что вы получите правильные решения для превосходных результатов. Свяжитесь с нашими экспертами сегодня, чтобы обсудить, как SiC может преобразить возможности вашей лаборатории!
Визуальное руководство
Связанные товары
- Карбид кремния (SiC) Керамический лист износостойкий инженерный передовой тонкой керамики
- Керамическая пластина из карбида кремния (SiC) для передовой тонкой керамики
- Керамический лист из карбида кремния (SiC) с плоским гофрированным радиатором для передовой тонкой технической керамики
- Нагревательные элементы из карбида кремния (SiC) для электрических печей
- Прецизионно обработанный лист нитрида кремния (SiN) для производства передовой тонкой керамики
Люди также спрашивают
- Каковы свойства и применение керамики из карбида кремния? Решение экстремальных инженерных задач
- Какова термостойкость карбида кремния? Выдерживает экстремальное нагревание до 1500°C
- Почему карбид кремния более эффективен? Добейтесь более высокой удельной мощности благодаря превосходным материальным свойствам SiC
- Какой бывает карбид кремния? Руководство по полиморфам, маркам и применению
- Каковы распространенные области применения карбида кремния? Раскройте экстремальную производительность в суровых условиях




