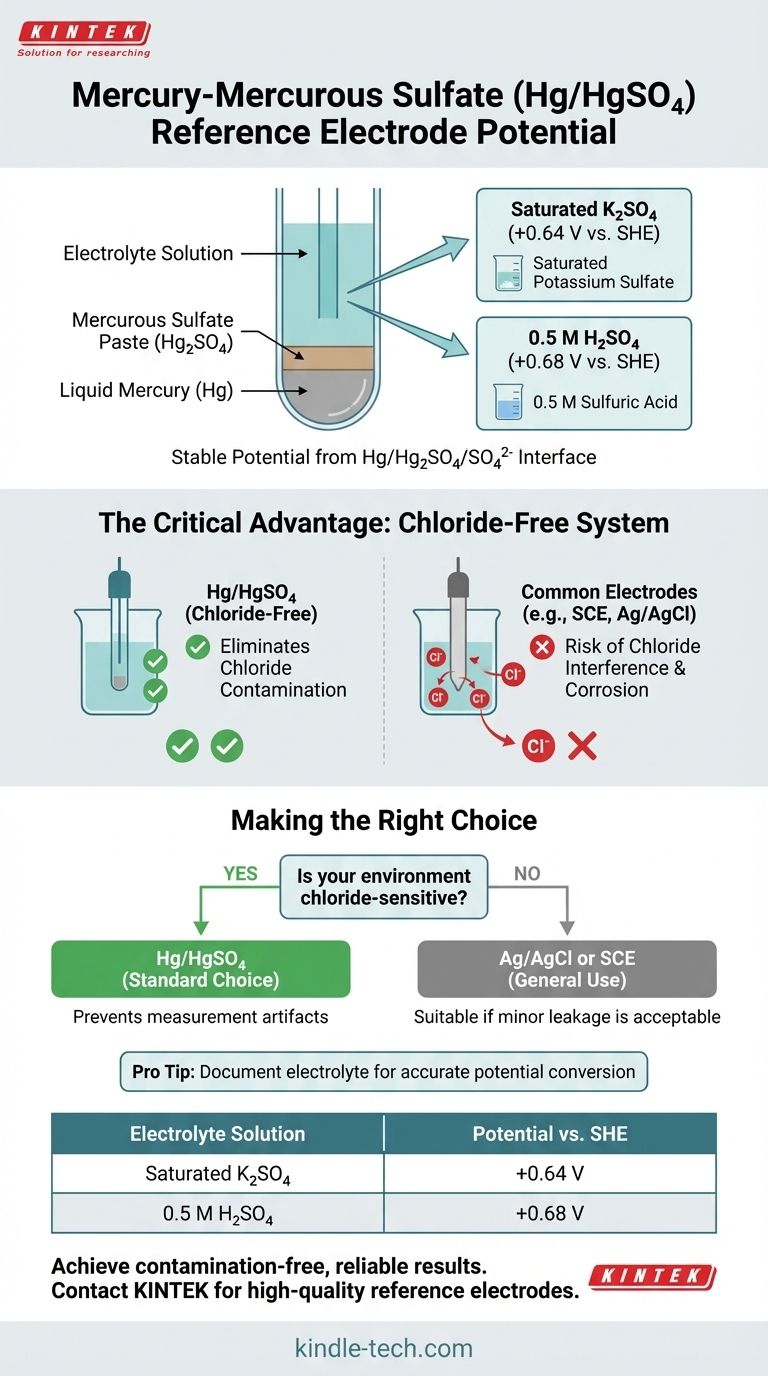
Принятый потенциал электрода сравнения ртуть/сульфат ртути(I) (Hg/Hg₂SO₄) обычно составляет +0,64 В относительно Стандартного водородного электрода (СВЭ) при использовании насыщенного раствора сульфата калия (K₂SO₄) в качестве электролита. Это значение немного меняется до +0,68 В относительно СВЭ при использовании электролита из 0,5 М серной кислоты (H₂SO₄).
Электрод Hg/Hg₂SO₄ — это специализированный, высокостабильный электрод сравнения, ценный по одной критической причине: он работает без ионов хлорида. Это делает его незаменимым выбором для электрохимических экспериментов, где загрязнение хлоридами может помешать результатам или повредить систему.

Что такое электрод ртуть/сульфат ртути(I)?
Основные компоненты
Электрод ртуть/сульфат ртути(I) состоит из слоя жидкой ртути (Hg), находящейся в непосредственном контакте с пастой из твердого сульфата ртути(I) (Hg₂SO₄).
Роль электролита
Эта паста из ртути и сульфата погружена в водный раствор, содержащий высокую концентрацию сульфатных ионов. Чаще всего это насыщенный раствор сульфата калия (K₂SO₄) или 0,5 М раствор серной кислоты (H₂SO₄).
Как он обеспечивает стабильный эталон
Граница раздела между ртутью, ее малорастворимой солью (Hg₂SO₄) и сульфатными ионами в электролите создает стабильную и воспроизводимую электрохимическую полуреакцию. Это равновесие генерирует постоянный потенциал, который служит надежным эталоном, относительно которого измеряется потенциал рабочего электрода.
Понимание его потенциала относительно СВЭ
Потенциал в сульфате калия (K₂SO₄)
При использовании насыщенного раствора сульфата калия в качестве заливочного раствора стандартный потенциал электрода Hg/Hg₂SO₄ составляет +0,64 В относительно Стандартного водородного электрода (СВЭ).
Потенциал в серной кислоте (H₂SO₄)
В кислой среде часто используется 0,5 М раствор серной кислоты в качестве заливочного раствора. Это немного сдвигает потенциал до +0,68 В относительно СВЭ. Изменение обусловлено различной активностью сульфатных ионов в двух электролитных растворах.
Критическое преимущество: система без хлоридов
Проблема с распространенными электродами
Наиболее широко используемые электроды сравнения, такие как насыщенный каломельный электрод (НКЭ) и электрод серебро/хлорид серебра (Ag/AgCl), заполнены концентрированными растворами хлорида калия (KCl).
Почему утечки хлорида вызывают беспокойство
Во время эксперимента незначительное количество этого богатого хлоридом заливочного раствора может просочиться из пористой перемычки электрода в ваш тестовый раствор. Это серьезная проблема в системах, где ионы хлорида могут мешать реакции, отравлять катализатор или вызывать коррозию компонентов из нержавеющей стали.
Решение Hg/Hg₂SO₄
Электрод Hg/Hg₂SO₄ был разработан специально для решения этой проблемы. Используя электролит на основе сульфата вместо хлорида, он полностью устраняет риск загрязнения хлоридами, обеспечивая целостность ваших измерений в чувствительных системах.
Сделайте правильный выбор для вашей цели
- Если ваша основная цель — работа в средах, чувствительных к хлоридам: Электрод Hg/Hg₂SO₄ является правильным и стандартным выбором для предотвращения артефактов измерения и повреждения системы.
- Если ваша основная цель — общая водная электрохимия: Более распространенный и часто менее дорогой электрод Ag/AgCl или НКЭ вполне подходит, при условии, что незначительная утечка хлорида допустима.
- Если ваша основная цель — преобразование потенциалов: Всегда указывайте конкретный электролит, используемый в вашем электроде Hg/Hg₂SO₄ (например, насыщенный K₂SO₄ или 0,5 М H₂SO₄), чтобы применить правильный коэффициент преобразования к шкале СВЭ.
Выбор подходящего электрода сравнения имеет фундаментальное значение для получения точных и надежных электрохимических данных.
Сводная таблица:
| Электролитный раствор | Потенциал относительно Стандартного водородного электрода (СВЭ) |
|---|---|
| Насыщенный сульфат калия (K₂SO₄) | +0,64 В |
| 0,5 М серная кислота (H₂SO₄) | +0,68 В |
Добивайтесь результатов без загрязнений и надежных результатов в ваших чувствительных электрохимических экспериментах. Электрод сравнения Hg/Hg₂SO₄ является окончательным выбором для применений, где ионы хлорида могут помешать вашей реакции, отравить катализатор или повредить вашу систему. KINTEK специализируется на предоставлении высококачественного лабораторного оборудования и расходных материалов, включая надежные электроды сравнения, для удовлетворения точных потребностей вашей лаборатории. Обеспечьте целостность ваших данных — свяжитесь с нашими экспертами сегодня, чтобы подобрать идеальный электрод сравнения для вашего исследования.
Визуальное руководство
Связанные товары
- Каломельный, хлорсеребряный, сульфатно-ртутный электрод сравнения для лабораторного использования
- Сульфатно-медный электрод сравнения для лабораторного использования
- Электрод из золотого листа для электрохимии
- Золотой дисковый электрод
- Графитовый дисковый стержневой и листовой электрод Электрохимический графитовый электрод
Люди также спрашивают
- Каково рекомендуемое обслуживание заполняющего раствора референсного электрода? Руководство по стабильным и точным показаниям
- Какой тип электрода можно использовать в качестве точки отсчета? Выберите правильный для точных измерений
- Какой электрод используется в качестве электрода сравнения для измерения полуэлементных потенциалов? Понимание универсального стандарта
- Какой электрод используется в качестве заземляющего электрода сравнения? Освойте ключ к точным электрохимическим измерениям
- Почему выбор высококачественного электрода сравнения имеет решающее значение в электрохимическом синтезе? | KINTEK















