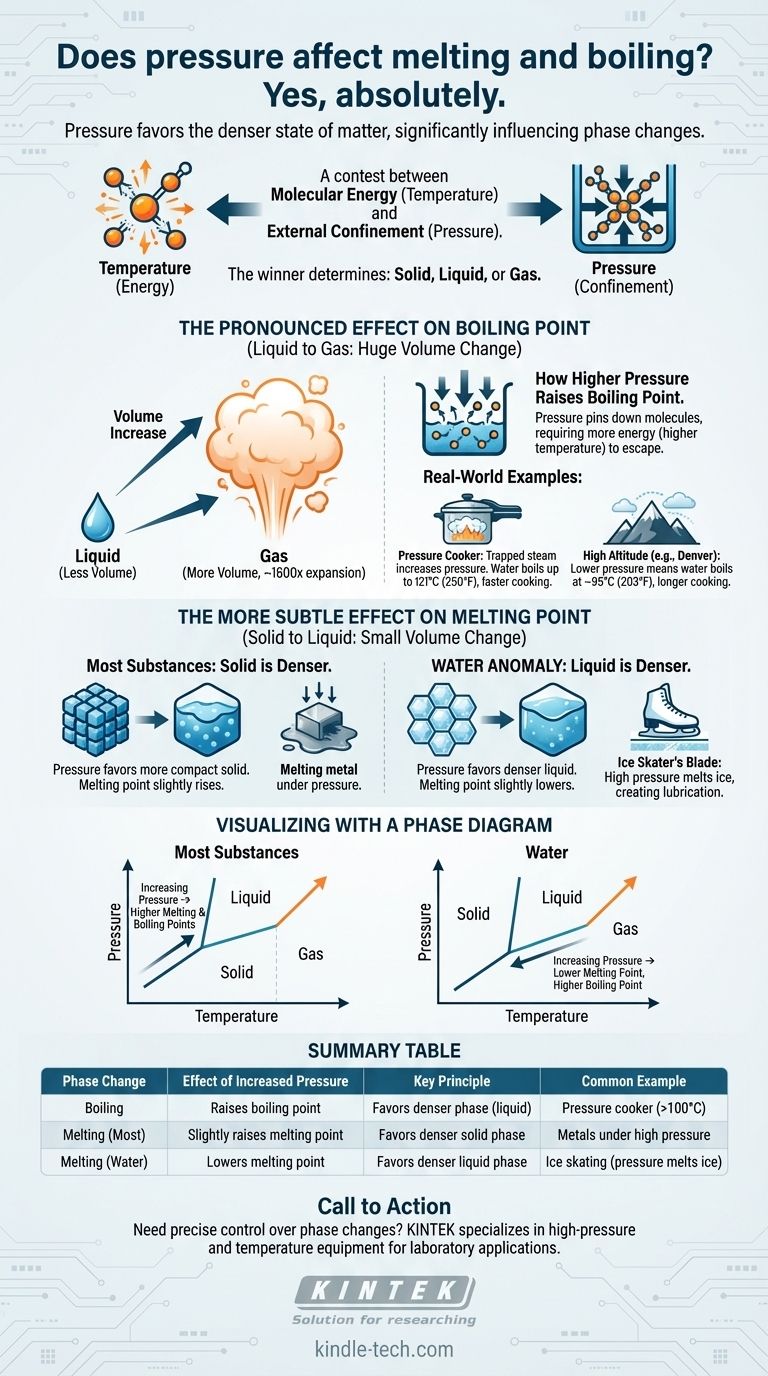
Да, безусловно. Давление является критическим фактором, который напрямую влияет на температуры, при которых вещества меняют фазу. Повышение внешнего давления, как правило, значительно повышает температуру кипения жидкости. Его влияние на температуру плавления более тонкое, но подчиняется четкому принципу: давление благоприятствует более плотному состоянию вещества.
Основной принцип — это соревнование между молекулярной энергией (температурой) и внешним ограничением (давлением). Температура дает молекулам энергию, чтобы вырваться в менее упорядоченное состояние, в то время как давление заставляет их сближаться в более компактное, плотное состояние. Победитель этого соревнования определяет, является ли вещество твердым телом, жидкостью или газом.

Почему давление влияет на фазовые переходы
Битва между энергией и ограничением
Фазовый переход, такой как плавление или кипение, происходит, когда молекулы получают достаточно тепловой энергии, чтобы преодолеть силы, удерживающие их в фиксированной структуре. Температура обеспечивает эту энергию.
Давление, с другой стороны, является внешней силой, сближающей молекулы. Оно действует как форма ограничения, затрудняя молекулам расширение и переход в менее плотную фазу.
Вопрос объема и плотности
Ключ к пониманию влияния давления кроется в объеме. Когда вещество плавится или кипит, его объем и плотность меняются.
Давление всегда будет благоприятствовать фазе, занимающей меньший объем, — более плотной фазе. Это одно правило объясняет, почему давление по-разному влияет на кипение и плавление.
Заметное влияние на температуру кипения
Из жидкости в газ: огромное изменение объема
Переход из жидкого состояния в газообразное включает в себя огромное увеличение объема. Например, одна капля воды расширяется, чтобы занять пространство, в более чем 1600 раз большее, когда она превращается в пар.
Поскольку это изменение объема настолько велико, давление оказывает очень сильное и прямое влияние на температуру кипения.
Как более высокое давление повышает температуру кипения
Когда вы увеличиваете давление на поверхность жидкости, вы, по сути, «прижимаете» молекулы. Теперь им требуется значительно больше кинетической энергии (более высокая температура), чтобы вырваться в газовую фазу.
Вот почему температура кипения почти всех веществ увеличивается с ростом давления.
Пример из реальной жизни: скороварка
Скороварка работает путем герметизации кастрюли и удержания пара, образующегося при кипении воды. Этот захваченный пар резко увеличивает давление внутри.
При таком высоком давлении температура кипения воды может подняться со 100°C (212°F) до 121°C (250°F). Эта более горячая вода быстрее передает тепло, резко сокращая время приготовления пищи.
Пример из реальной жизни: приготовление пищи на большой высоте
Противоположное происходит на больших высотах. В Денвере, штат Колорадо (на высоте 5280 футов), атмосферное давление ниже.
Поскольку атмосферное давление меньше удерживает молекулы воды, они легче переходят в газообразное состояние. Вода там кипит при температуре около 95°C (203°F), а это означает, что пищу приходится готовить дольше.
Более тонкое влияние на температуру плавления
Из твердого тела в жидкость: небольшое изменение объема
В отличие от кипения, изменение объема при плавлении очень мало. Плотности вещества в твердом и жидком состоянии, как правило, очень схожи.
Поскольку изменение объема минимально, давление оказывает гораздо менее драматичное влияние на температуру плавления.
Для большинства веществ: повышение давления повышает температуру плавления
Большинство материалов — от металлов до восков и углекислого газа — более плотные в твердом состоянии, чем в жидком.
В этих случаях увеличение давления благоприятствует более компактному твердому состоянию. Это немного затрудняет плавление, поэтому требуется более высокая температура. Температура плавления повышается с ростом давления.
Аномалия воды: решающее исключение
Вода — замечательное и редкое исключение. Твердая вода (лед) менее плотная, чем жидкая вода, поэтому лед плавает.
Поскольку жидкая вода является более плотной фазой, увеличение давления на лед способствует образованию жидкости. Это означает, что под высоким давлением лед будет плавиться при температуре ниже 0°C (32°F).
Пример из реальной жизни: лезвие конька
Классическая иллюстрация этого принципа — фигурист. Тонкое лезвие конька концентрирует весь вес фигуриста на крошечной площади, создавая огромное давление на лед.
Это высокое давление заставляет лед непосредственно под лезвием плавиться при немного более низкой температуре, создавая микроскопический слой воды, который смазывает путь лезвия.
Понимание компромиссов: визуализация с помощью фазовой диаграммы
Фазовая диаграмма — это простая карта, показывающая состояние вещества (твердое, жидкое или газообразное) при любой комбинации температуры и давления.
Граница жидкость-газ
Линия, разделяющая жидкую и газообразную фазы, всегда наклонена вверх и вправо. Это наглядно подтверждает, что при увеличении давления (движение вверх по вертикальной оси) вы также должны увеличивать температуру (движение вправо по горизонтальной оси), чтобы вещество закипело.
Граница твердое тело-жидкость
Линия между твердой и жидкой фазами почти вертикальна, что показывает, что давление оказывает гораздо меньшее влияние на плавление.
Для большинства веществ эта линия слегка наклонена вправо (более высокое давление, более высокая температура плавления). Для воды эта линия уникально наклонена влево, показывая, что более высокое давление приводит к более низкой температуре плавления.
Ключевые принципы для практического применения
Чтобы эффективно применять эти знания, сосредоточьтесь на веществе и типе фазового перехода.
- Если вы имеете дело с кипением или конденсацией: Помните, что давление является доминирующим фактором. Более высокое давление означает более высокую температуру кипения, а более низкое давление означает более низкую температуру кипения.
- Если вы имеете дело с плавлением или замерзанием (для большинства материалов): Влияние давления незначительно. Более высокое давление немного повысит температуру плавления, благоприятствуя более плотному твердому состоянию.
- Если вы имеете дело конкретно с водяным льдом: Помните, что это исключение. Более высокое давление понижает температуру замерзания/плавления, благоприятствуя более плотному жидкому состоянию.
Понимание того, как взаимодействуют давление и температура, дает вам прямой контроль над физическим состоянием материи.
Сводная таблица:
| Фазовый переход | Влияние повышенного давления | Ключевой принцип | Общий пример |
|---|---|---|---|
| Кипение | Повышает температуру кипения | Способствует более плотной фазе (жидкость) | Скороварка (вода кипит при >100°C) |
| Плавление (большинство материалов) | Слегка повышает температуру плавления | Способствует более плотной твердой фазе | Металлы под высоким давлением |
| Плавление (вода/лед) | Понижает температуру плавления | Способствует более плотной жидкой фазе | Катание на коньках (давление плавит лед) |
Нужен точный контроль фазовых переходов в ваших лабораторных процессах? KINTEK специализируется на оборудовании для высокого давления и температуры для лабораторных применений. Независимо от того, разрабатываете ли вы новые материалы, проводите химический синтез или изучаете фазовое поведение, наши реакторы и печи обеспечивают точный контроль давления и температуры, который вам нужен. Свяжитесь с нашими экспертами сегодня, чтобы обсудить, как наши решения могут повысить эффективность и точность ваших исследований.
Визуальное руководство