При выборе электролита для эксперимента необходимо оценить четыре ключевых свойства: его ионную проводимость, электрохимическое окно стабильности, его растворимость в выбранном растворителе и его химическую совместимость со всей вашей экспериментальной системой. Эти факторы в совокупности определяют, будет ли электролит поддерживать реакцию, которую вы хотите изучить, или вносить артефакты, которые ставят под сомнение ваши результаты.
Основной вывод заключается в том, что электролит — это не просто пассивный проводник. Это активный химический компонент, который определяет рабочие пределы вашей электрохимической ячейки и может напрямую участвовать в побочных реакциях, что делает его тщательный выбор основополагающим для получения надежных и значимых данных.

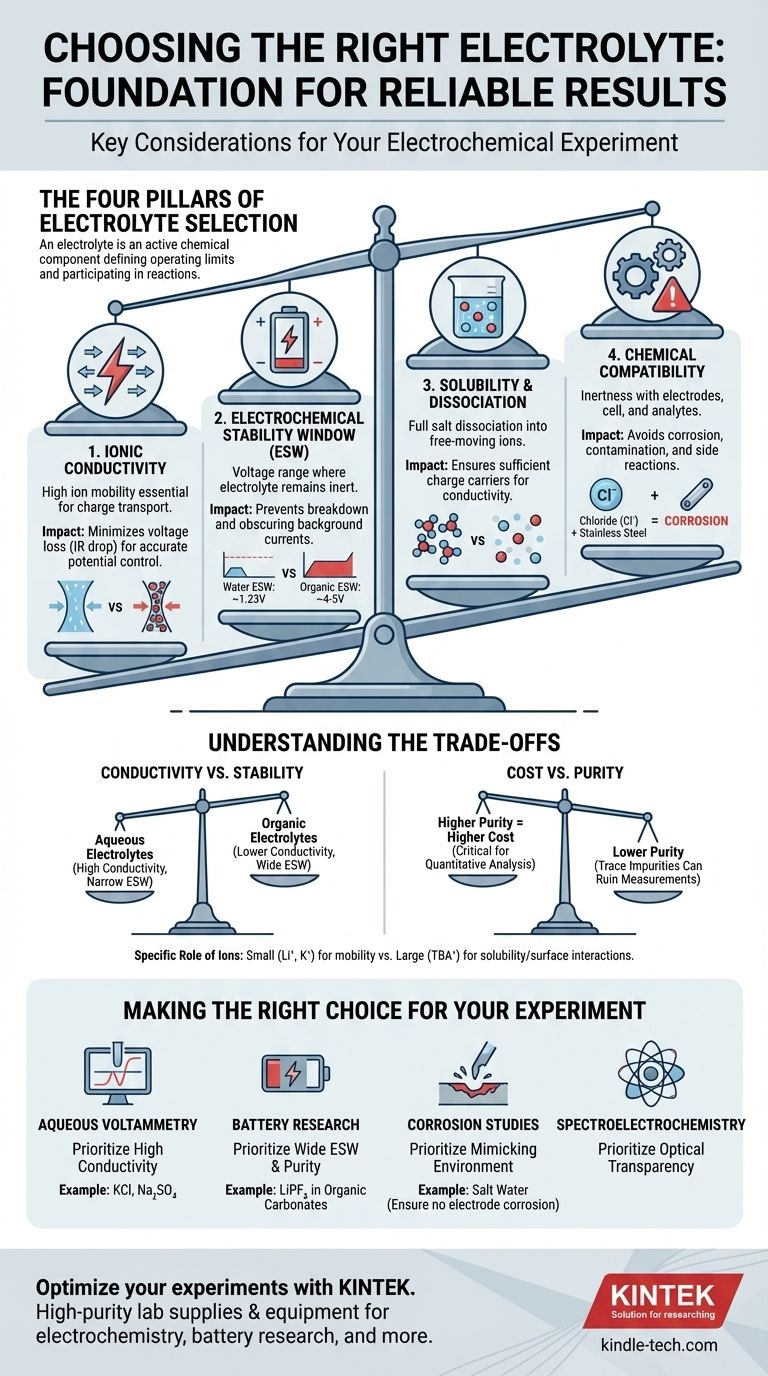
Четыре столпа выбора электролита
Выбор правильного электролита — это процесс балансировки требований. Идеальный электролит облегчает желаемую реакцию, оставаясь при этом совершенно инертным и невидимым для измерения. Мы можем разбить этот процесс выбора на четыре критических аспекта.
Столп 1: Ионная проводимость
Основная задача электролита — переносить заряд между электродами. Для этого необходима высокая ионная проводимость.
Плохая проводимость приводит к большому омическому падению (или IR-падению) — потере напряжения в электролите. Это означает, что потенциал, который вы прикладываете к ячейке, не является потенциалом, который фактически ощущается на поверхности электрода, что приводит к неточным измерениям потенциалов реакции.
Представьте себе электролит как шоссе для ионов. Электролит с высокой проводимостью — это широкое, свободное скоростное шоссе, а с низкой проводимостью — загруженная второстепенная дорога, замедляющая все и расходующая энергию.
Столп 2: Электрохимическое окно стабильности (ЭОС)
Электрохимическое окно стабильности (ЭОС) — это диапазон потенциалов, в котором сам электролит — как соль, так и растворитель — не окисляется и не восстанавливается.
Работа за пределами этого окна является критической ошибкой. Если вы приложите слишком положительный или слишком отрицательный потенциал, вы начнете разрушать электролит, а не изучать аналит. Это создает большие фоновые токи, которые могут полностью замаскировать сигнал, который вы пытаетесь измерить.
Например, ЭОС воды составляет всего около 1,23 В. Для экспериментов, требующих более высоких потенциалов, например, в исследованиях литий-ионных аккумуляторов, необходимо перейти на органические растворители и специальные соли (например, LiPF₆ в органических карбонатах), которые обеспечивают гораздо более широкое окно (~4–5 В).
Столп 3: Растворимость и диссоциация
Чтобы электролит функционировал, соль должна не только раствориться, но и полностью диссоциировать на свободно движущиеся катионы и анионы в растворителе.
Если соль плохо растворяется или образует прочные «ионные пары» вместо разделения, количество доступных переносчиков заряда резко снижается. Это напрямую снижает ионную проводимость, подрывая основную функцию электролита.
Всегда убеждайтесь, что выбранная вами соль хорошо растворима в выбранном растворителе в той концентрации, которую вы планируете использовать (обычно от 0,1 М до 1,0 М для лабораторных экспериментов).
Столп 4: Химическая совместимость
Электролит должен быть химически инертен по отношению к каждому компоненту вашей ячейки: рабочему электроду, противоэлектроду, опорному электроду и самому корпусу ячейки.
Распространенная ошибка — использование электролита, содержащего ионы хлорида (например, KCl), с компонентами из нержавеющей стали. Хлорид сильно коррозирует нержавеющую сталь и вызовет точечную коррозию и высвобождение ионов металлов в ваш раствор, загрязняя эксперимент.
Аналогичным образом, ионы электролита не должны вступать в реакцию или слишком сильно адсорбироваться на поверхности вашего электрода, если только это взаимодействие не является тем конкретным явлением, которое вы изучаете.
Понимание компромиссов
Не существует единственного «лучшего» электролита; каждый выбор включает в себя балансировку конкурирующих факторов. Понимание этих компромиссов — признак опытного исследователя.
Проводимость против стабильности
Водные электролиты (например, NaCl в воде) обеспечивают отличную ионную проводимость, но имеют очень узкое электрохимическое окно стабильности. И наоборот, многие электролиты на основе органических растворителей обеспечивают широкое окно стабильности, но часто страдают от более низкой проводимости. Ваш выбор зависит от того, ограничена ли ваша экспериментальная установка напряжением или эффективностью по току.
Стоимость против чистоты
Соли и растворители высокой чистоты, «аккумуляторного» или «электрохимического» класса значительно дороже. Однако следовые примеси (например, вода в неводном электролите или галогенид-ионы) могут вносить нежелательные электрохимические сигналы и портить чувствительные измерения. Для простых демонстраций может быть достаточно более низкого сорта, но для количественного анализа инвестиции в чистоту критически важны.
Особая роль ионов
Не все ионы одинаковы. Малые, подвижные ионы, такие как литий (Li⁺) или калий (K⁺), являются отличными переносчиками заряда. Однако крупные органические ионы, такие как тетрабутиламмоний (TBA⁺), часто используются для увеличения растворимости неполярных аналитов в полярных растворителях и могут помочь минимизировать нежелательные взаимодействия на поверхности электрода.
Принятие правильного решения для вашего эксперимента
Ваша конкретная цель диктует, каким свойствам следует отдать приоритет.
- Если ваш основной фокус — стандартная водная вольтамперометрия: Отдавайте приоритет высокой проводимости и используйте простую, инертную соль, такую как хлорид калия (KCl) или сульфат натрия (Na₂SO₄), убедившись, что ваш диапазон потенциалов остается в пределах окна стабильности воды.
- Если ваш основной фокус — исследования высоковольтных аккумуляторов: Отдавайте приоритет широкому электрохимическому окну стабильности и экстремальной чистоте, обычно используя такие соли, как LiPF₆ или LiClO₄ в смеси органических карбонатных растворителей.
- Если ваш основной фокус — коррозионные исследования: Отдавайте приоритет созданию электролита, который точно имитирует реальную среду (например, соленую воду), при этом гарантируя, что он не вызывает коррозии ваших опорных или противоэлектродов.
- Если ваш основной фокус — спектроэлектрохимия: В дополнение к стандартным электрохимическим требованиям отдавайте приоритет оптической прозрачности как соли, так и растворителя в желаемом диапазоне длин волн.
В конечном счете, выбранный вами электролит задает сцену и определяет правила для всего вашего электрохимического измерения.
Сводная таблица:
| Столп выбора | Ключевой аспект | Влияние на эксперимент |
|---|---|---|
| Ионная проводимость | Высокая подвижность ионов | Минимизирует потерю напряжения (IR-падение) для точного контроля потенциала. |
| Электрохимическое окно стабильности (ЭОС) | Диапазон напряжения стабильности | Предотвращает разрушение электролита и маскировку фоновыми токами. |
| Растворимость и диссоциация | Полная диссоциация соли на ионы | Обеспечивает достаточное количество переносчиков заряда для эффективной проводимости. |
| Химическая совместимость | Инертность по отношению к компонентам ячейки | Предотвращает коррозию, загрязнение и нежелательные побочные реакции. |
Готовы оптимизировать свои электрохимические эксперименты с помощью правильного лабораторного оборудования и расходных материалов? Правильный электролит — лишь часть уравнения. KINTEK специализируется на поставке высокочистых лабораторных принадлежностей и оборудования, адаптированных для электрохимии, исследований аккумуляторов, коррозионных исследований и многого другого. Наша продукция помогает вам достичь точного контроля и надежных данных, требуемых вашей работой.
Свяжитесь с нашими экспертами сегодня, чтобы обсудить ваши конкретные потребности в применении и узнать, как KINTEK может поддержать успех вашей лаборатории.
Визуальное руководство
Связанные товары
- Электрохимическая ячейка с пятью портами
- Супергерметичная электрохимическая электролитическая ячейка
- Электрохимическая ячейка для оценки покрытий
- Протонпроводящая мембрана для лабораторных применений в батареях
- Электрохимическая ячейка с газодиффузионным электролизом и ячейка для реакции с протоком жидкости
Люди также спрашивают
- Какие материалы используются для корпуса супергерметичной электролитической ячейки и каковы их свойства? Выберите правильный материал для вашего эксперимента
- Как конструкция электролитической ячейки влияет на выход феррата(VI)? Оптимизация эффективности и чистоты
- Каковы три основных компонента электролитической ячейки? Ключевые элементы химического синтеза
- Каковы основные правила техники безопасности при использовании электролитической ячейки? Основные протоколы безопасности в лаборатории
- Как предотвратить короткие замыкания в установке электролитической ячейки? Важные советы по безопасности и производительности



















