Говоря прямо, гальванический элемент не отличается от электрохимической ячейки — это тип электрохимической ячейки. Термин «электрохимическая ячейка» является широкой категорией для любого устройства, которое преобразует химическую энергию в электрическую или наоборот. Гальванический элемент, также известный как вольтов элемент, является специфическим типом, который спонтанно генерирует электричество из химической реакции.
Основное заблуждение возникает из-за того, что эти термины рассматриваются как параллельные варианты. Вместо этого думайте об этом как об иерархии: «Электрохимическая ячейка» — это название семейства, и у него есть два «ребенка»: Гальванический элемент (который производит энергию) и Электролитическая ячейка (который потребляет энергию).

Два пути электрохимии
Электрохимическая ячейка — это, по сути, мост между химическим и электрическим мирами. Все такие ячейки имеют общие основные компоненты — два электрода (анод и катод) и электролит, который позволяет ионам перемещаться между ними.
Ключевое различие заключается в направлении преобразования энергии.
Тип 1: Гальванический (вольтов) элемент — спонтанное выделение энергии
Гальванический элемент использует спонтанную химическую реакцию для производства электрической энергии.
Представьте это как контролируемый спуск. Химические вещества естественным образом находятся «под горой» с точки зрения энергии, и гальванический элемент обеспечивает путь для высвобождения этой энергии в виде полезного электрического тока.
Это принцип работы обычной батареи. Химические реакции внутри батарейки типа АА хотят произойти сами по себе, и когда вы замыкаете цепь, элемент направляет полученный поток электронов для питания вашего устройства.
Тип 2: Электролитическая ячейка — вынужденное химическое изменение
Электролитическая ячейка делает прямо противоположное. Она использует внешний источник электрической энергии для принудительного осуществления химической реакции, которая не произошла бы сама по себе.
Это «восходящий» путь. Вы вводите энергию в систему, чтобы создать менее стабильное химическое состояние.
Классические примеры включают использование электричества для электролиза (например, расщепление воды на водород и кислород) или перезарядку батареи. Когда вы заряжаете свой телефон, вы используете его батарею как электролитическую ячейку, обращая химические реакции, которые происходили, когда она питала ваше устройство.
Понимание критических различий
Различие между этими двумя типами ячеек является наиболее важной концепцией в базовой электрохимии. Направление потока энергии определяет всю функцию ячейки.
Преобразование энергии
Гальванический элемент преобразует химическую энергию в электрическую. Это источник энергии.
Электролитическая ячейка преобразует электрическую энергию в химическую. Это потребитель энергии.
Спонтанность реакции
Окислительно-восстановительная реакция в гальваническом элементе является спонтанной. Она происходит без внешнего вмешательства после замыкания цепи.
Окислительно-восстановительная реакция в электролитической ячейке является неспонтанной. Для ее протекания требуется внешний источник питания (например, батарея или источник постоянного тока).
Практическая функция
Функция гальванического элемента — питать что-либо. Подумайте о любой стандартной, неперезаряжаемой батарее.
Функция электролитической ячейки — вызывать химическое изменение. Подумайте об гальванопластике металла или зарядке перезаряжаемой батареи.
Как правильно классифицировать вашу ячейку
Чтобы применить эти знания, просто спросите, производит ли ячейка энергию или потребляет ее для запуска реакции.
- Если ваша основная цель — описать любое устройство, которое взаимопреобразует химическую и электрическую энергию: Используйте широкий термин электрохимическая ячейка.
- Если вы конкретно описываете батарею, которая разряжается для питания устройства: Используйте конкретные термины гальванический элемент или вольтов элемент.
- Если вы конкретно описываете процесс, который использует электричество для принудительного осуществления реакции (например, зарядка батареи или электролиз): Используйте конкретный термин электролитическая ячейка.
Понимая эту простую классификацию, вы сможете описывать любой электрохимический процесс с точностью и ясностью.
Сводная таблица:
| Характеристика | Гальванический/Вольтов элемент | Электролитическая ячейка |
|---|---|---|
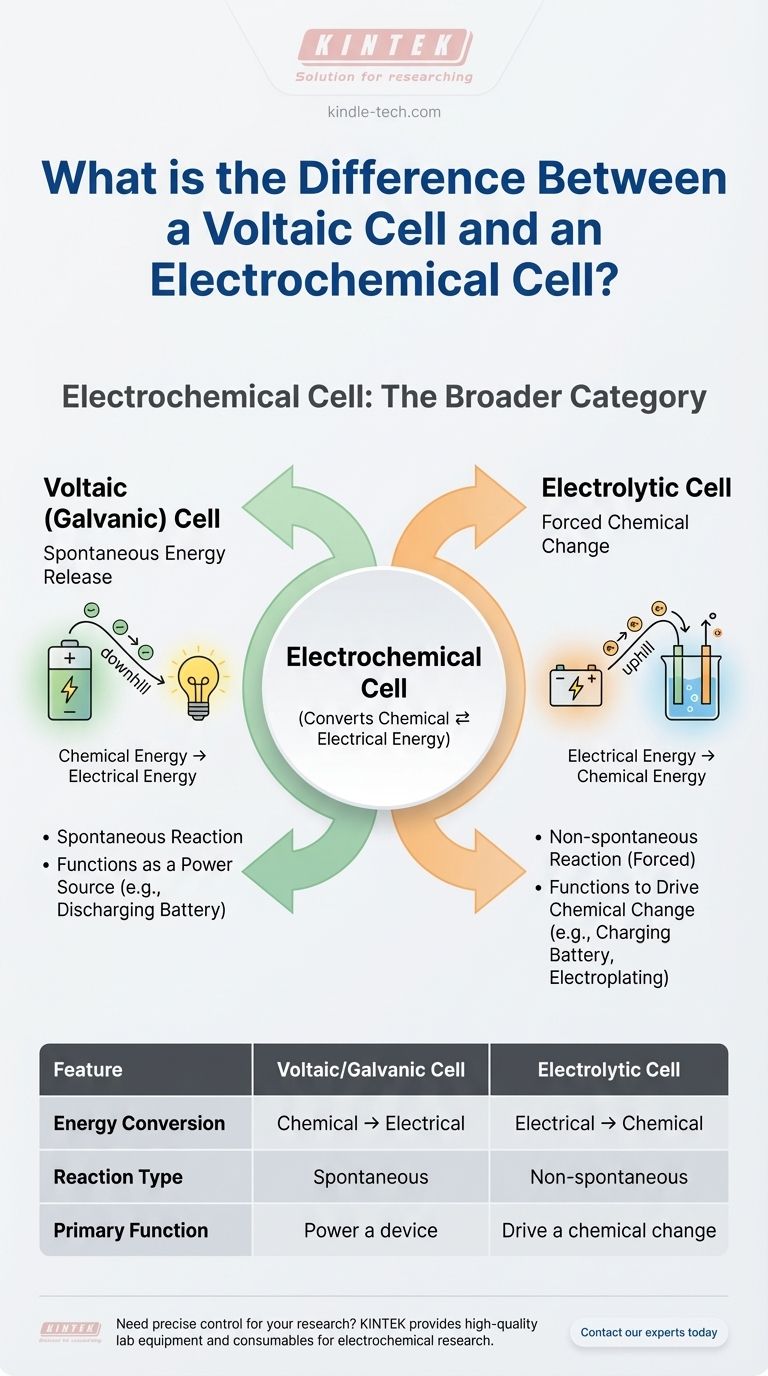
| Преобразование энергии | Химическая → Электрическая | Электрическая → Химическая |
| Тип реакции | Спонтанная | Неспонтанная (вынужденная) |
| Основная функция | Питание устройства (например, батареи) | Вызов химического изменения (например, гальванопластика) |
Нужен точный контроль над вашими электрохимическими процессами? KINTEK специализируется на высококачественном лабораторном оборудовании и расходных материалах для всех ваших электрохимических исследований и разработок. Независимо от того, работаете ли вы с гальваническими элементами, электролитическими ячейками или любым другим лабораторным применением, наши решения обеспечивают точность и надежность. Свяжитесь с нашими экспертами сегодня, чтобы найти идеальное оборудование для вашей лаборатории!
Визуальное руководство
Связанные товары
- Электрохимическая ячейка для оценки покрытий
- Электрохимическая ячейка с пятью портами
- Двухслойная оптическая электролитическая электрохимическая ячейка H-типа с водяной баней
- Оптическая электрохимическая ячейка с боковым окном
- Электрохимическая ячейка из ПТФЭ, коррозионностойкая, герметичная и негерметичная
Люди также спрашивают
- Как конструкция электрохимической электролизной ячейки влияет на равномерность покрытия? Оптимизируйте свои катализаторы
- Какова процедура начала эксперимента и что следует наблюдать? Пошаговое руководство для надежной электрохимии
- Почему электрохимическую ячейку необходимо постоянно продувать азотом? Обеспечение точности тестов на коррозию Ni-Cr
- В чем разница между электролитом и электродом в ячейке? Освойте основы электрохимических систем
- Как стандартизированная электрохимическая испытательная ячейка помогает в скрининге электродов MOx/CNTf? Оптимизация соотношения материалов



















