Для лабораторных применений корпус электролитической ячейки обычно изготавливается из высокоборосиликатного стекла, часто с толщиной стенки около 4,5–5 мм. Этот материал выбирается за его химическую инертность и термостойкость. Однако физический сосуд — это лишь часть более крупной системы, предназначенной для проведения химической реакции с использованием электричества.
Корпус ячейки — это просто инертный сосуд. Истинная функция электролитической ячейки определяется ее тремя основными внутренними компонентами: двумя электродами (анодом и катодом), электролитом, содержащим подвижные ионы, и внешним источником питания для запуска реакции.

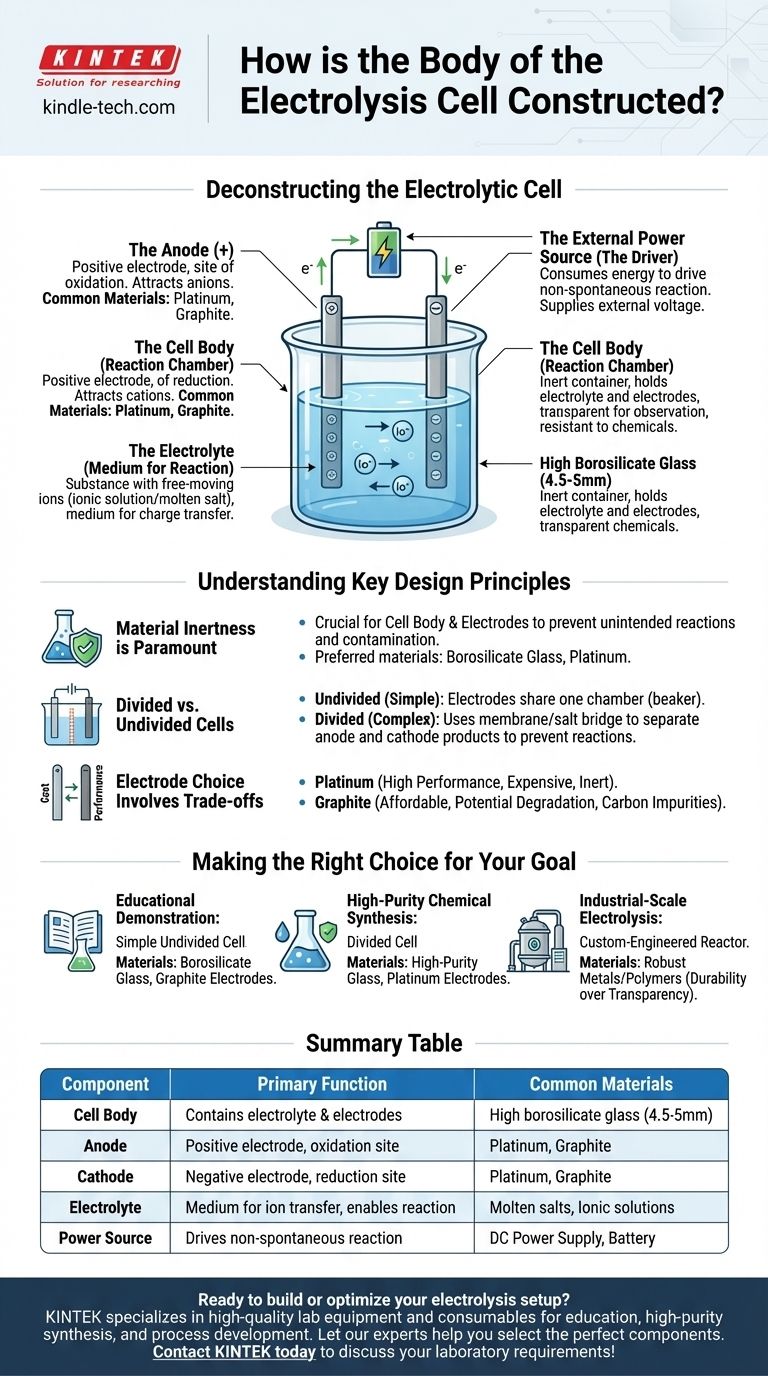
Деконструкция электролитической ячейки
Чтобы понять конструкцию ячейки, необходимо выйти за рамки физического сосуда и проанализировать функциональные компоненты, которые он содержит. Электролитическая ячейка представляет собой полную систему, где каждая часть играет критически важную роль в процессе электролиза.
Корпус ячейки (Реакционная камера)
Основная функция корпуса заключается в удержании электролита и фиксации электродов на месте, не вмешиваясь в химическую реакцию.
Высокоборосиликатное стекло является распространенным материалом, поскольку оно прозрачно, что позволяет проводить наблюдения, и высокоустойчиво к коррозии от часто агрессивных химикатов, используемых в качестве электролитов. Для специфических применений могут использоваться и другие инертные материалы, такие как определенные полимеры.
Электроды (Анод и Катод)
Электроды — это проводники, которые вводят электрическую энергию в систему. В электролитической ячейке их всегда два.
- Анод — это положительный электрод. Он притягивает отрицательно заряженные ионы (анионы), и именно здесь происходит окисление.
- Катод — это отрицательный электрод. Он притягивает положительно заряженные ионы (катионы), и именно здесь происходит восстановление.
Они обычно изготавливаются из инертных материалов, таких как платина или графит, которые хорошо проводят электричество, но сами не вступают в химическую реакцию.
Электролит (Среда для реакции)
Электролит — это вещество, содержащее свободно движущиеся ионы и заполняющее корпус ячейки. Это среда, через которую происходит перенос заряда между электродами.
Электролитами могут быть ионное соединение, растворенное в растворителе (например, соль в воде), или расплавленное ионное соединение (например, расплавленный хлорид натрия). Именно ионы, присутствующие в электролите, будут окисляться или восстанавливаться в процессе электролиза.
Внешний источник питания (Двигатель)
В отличие от батареи, которая производит энергию, электролитическая ячейка потребляет энергию, чтобы заставить протекать несамопроизвольную реакцию.
Эта энергия подается от внешнего источника питания, такого как батарея или источник постоянного тока, который подключается к аноду и катоду. Это внешнее напряжение заставляет электроны проходить через цепь и направляет ионы к соответствующим электродам.
Понимание ключевых принципов проектирования
Конструкция электролитической ячейки руководствуется фундаментальными принципами, обеспечивающими ее правильное функционирование. Непонимание этих принципов может привести к неудачным экспериментам или неэффективным процессам.
Химическая инертность имеет первостепенное значение
Самый важный принцип для корпуса ячейки и электродов — это химическая инертность. Сосуд и электрические проводники не должны вступать в реакцию с электролитом. Любая непреднамеренная реакция может загрязнить продукты и нарушить желаемый электрохимический процесс. Именно поэтому специализированные материалы, такие как боросиликатное стекло и платина, предпочтительнее обычного стекла или реактивных металлов.
Разделенные и неразделенные ячейки
Самая простая конструкция ячейки — это «неразделенная» ячейка, где оба электрода находятся в общем электролите в одной камере, например, в стакане.
Однако иногда продукты, образующиеся на аноде и катоде, могут реагировать друг с другом. В таких случаях используется «разделенная» ячейка. Эта конструкция включает пористую мембрану или солевой мостик для разделения ячейки на две отдельные полуячейки, изолируя продукты, но позволяя ионам проходить между отсеками.
Выбор электрода сопряжен с компромиссами
Хотя и платина, и графит распространены, выбор между ними включает классический компромисс между стоимостью и производительностью.
Платина чрезвычайно инертна и эффективна, но очень дорога. Графит является гораздо более доступным проводником, но может разрушаться или вступать в реакцию при определенных условиях, особенно при высоких напряжениях или с определенными электролитами, что потенциально может привести к попаданию примесей углерода в систему.
Сделайте правильный выбор для вашей цели
Оптимальная конструкция электролитической ячейки полностью зависит от ее предполагаемого применения.
- Если ваш основной фокус — образовательная демонстрация: Простой неразделенный стакан из боросиликатного стекла с недорогими графитовыми электродами вполне достаточен и экономичен.
- Если ваш основной фокус — высокочистый химический синтез: Разделенная ячейка из высокочистого стекла с устойчивыми, инертными платиновыми электродами необходима для предотвращения загрязнения продуктов и побочных реакций.
- Если ваш основной фокус — электролиз в промышленных масштабах: Ячейка будет представлять собой высокоспециализированный, индивидуально спроектированный реактор, часто изготовленный из прочных металлов или полимеров, предназначенных для долговечности, эффективности и непрерывной работы, а не для прозрачности.
Понимание этих основных компонентов и их функций позволяет вам выбрать или спроектировать ячейку, которая точно соответствует вашей цели.
Сводная таблица:
| Компонент | Основная функция | Распространенные материалы |
|---|---|---|
| Корпус ячейки | Содержит электролит и электроды | Высокоборосиликатное стекло (4,5–5 мм) |
| Анод | Положительный электрод; место окисления | Платина, Графит |
| Катод | Отрицательный электрод; место восстановления | Платина, Графит |
| Электролит | Среда для переноса ионов; обеспечивает реакцию | Расплавленные соли, Ионные растворы |
| Источник питания | Запускает несамопроизвольную реакцию | Источник постоянного тока, Батарея |
Готовы построить или оптимизировать вашу установку для электролиза? Правильная конструкция ячейки имеет решающее значение для успеха вашей лаборатории, будь то для образования, высокочистого синтеза или разработки процессов. KINTEK специализируется на предоставлении высококачественного лабораторного оборудования и расходных материалов, которые вам нужны — от прочной боросиликатной посуды до инертных платиновых и графитовых электродов. Позвольте нашим экспертам помочь вам выбрать идеальные компоненты для вашего конкретного применения. Свяжитесь с KINTEK сегодня, чтобы обсудить ваши лабораторные потребности!
Визуальное руководство
Связанные товары
- Настраиваемые электролизеры PEM для различных исследовательских применений
- Электрохимическая ячейка для спектроэлектролиза в тонком слое
- Электрохимическая ячейка с газодиффузионным электролизом и ячейка для реакции с протоком жидкости
- Кварцевая электрохимическая ячейка для электрохимических экспериментов
- Электрохимическая ячейка из ПТФЭ, коррозионностойкая, герметичная и негерметичная
Люди также спрашивают
- Как еще называют электролитическую ячейку? Понимание электролитических и гальванических ячеек
- Каковы риски неправильного контроля напряжения в электролитической ячейке? Избегайте дорогостоящих повреждений и неэффективности
- Какова правильная процедура отключения эксперимента по электролизу после его завершения? Пошаговое руководство по безопасности
- Какие параметры должны строго контролироваться в процессе электролиза? Обеспечьте точность и эффективность
- Какова немедленная процедура очистки электролизной ячейки после использования? Предотвратите накопление отложений для получения точных результатов



















