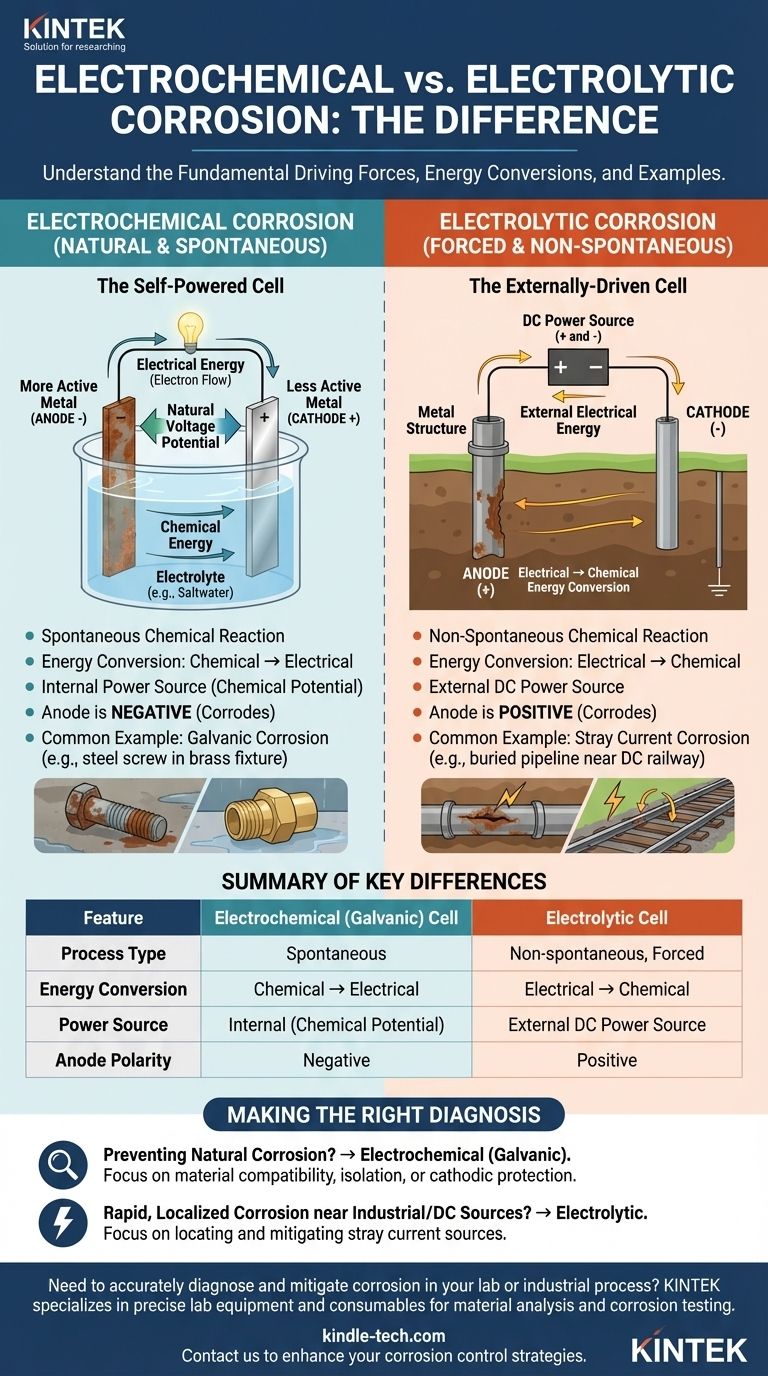
На фундаментальном уровне разница между электролитическим и электрохимическим коррозионным элементом заключается в их преобразовании энергии и движущей силе. Электрохимический элемент — это спонтанный процесс, который преобразует запасенную химическую энергию в электрическую, вызывая естественную коррозию. Напротив, электролитический элемент — это неспонтанный процесс, который использует внешнюю электрическую энергию для принудительного протекания химической реакции, вызывая индуцированную коррозию.
Основное различие — спонтанность. Электрохимическая коррозия происходит естественным образом сама по себе, как разрядка батареи. Электролитическая коррозия навязывается материалу внешним источником питания, например, блуждающим постоянным током от железнодорожной системы.

Электрохимический элемент: естественное состояние коррозии
Электрохимический элемент, часто называемый гальваническим элементом, является механизмом, лежащим в основе наиболее распространенных форм коррозии. Это самодостаточный, естественно протекающий процесс.
Спонтанная химическая реакция
Этот тип элемента образуется, когда два разных металла находятся в электрическом контакте в присутствии электролита (например, соленой воды). Между ними существует естественный потенциал напряжения.
Более химически активный металл становится анодом (отрицательным электродом) и корродирует, высвобождая электроны. Менее активный металл становится катодом (положительным электродом) и принимает эти электроны.
Преобразование энергии: химическая в электрическую
Движущей силой является высвобождение запасенной химической энергии в более активном металле. Эта химическая энергия преобразуется непосредственно в электрическую энергию в виде потока электронов от анода к катоду. Этот процесс не требует внешнего питания.
Классическим примером является гальваническая коррозия, когда стальной винт (анод) быстро ржавеет при соединении с латунным креплением (катод) во влажной среде.
Электролитический элемент: коррозия под принуждением
Электролитический элемент вызывает химическую реакцию, которая в обычных условиях не произошла бы. Это достигается путем подачи внешнего источника электрической энергии.
Неспонтанная химическая реакция
Этот процесс преодолевает естественные тенденции задействованных материалов. Внешний источник питания заставляет металл становиться анодом и корродировать, даже если в противном случае он был бы стабилен.
Коррозия происходит там, где этот внешний постоянный ток (DC) покидает металлическую конструкцию и входит в электролит.
Преобразование энергии: электрическая в химическую
Здесь электрическая энергия от внешнего источника преобразуется в химическую энергию, которая проявляется в виде реакции коррозии. Элемент потребляет энергию для работы.
Распространенным реальным сценарием является коррозия блуждающими токами. Закопанный трубопровод, проходящий рядом с железной дорогой, питаемой постоянным током, может улавливать утекающий ток, заставляя участок трубы, где ток выходит обратно в почву, корродировать с ускоренной скоростью.
Понимание ключевых различий
Хотя оба процесса включают аноды, катоды и электролит, их фундаментальные характеристики противоположны. Признание этих различий имеет решающее значение для правильной диагностики и смягчения последствий.
Движущая сила и источник питания
Наиболее важным отличием является движущая сила. Электрохимический элемент самопитается за счет разности химических потенциалов между материалами. Электролитический элемент питается извне от внешнего источника постоянного тока.
Полярность электродов
Полярность анода и катода меняется местами между двумя элементами, что часто вызывает путаницу.
- В электрохимическом (гальваническом) элементе анод (где происходит коррозия) является отрицательным, а катод — положительным.
- В электролитическом элементе внешний источник питания делает анод (где происходит коррозия) положительным, а катод — отрицательным.
Практические последствия
Неправильное определение типа коррозионного элемента приводит к неверным решениям. Например, изменение пар материалов может решить проблему гальванической коррозии, но ничего не сделает для остановки коррозии блуждающими токами.
Правильная диагностика
Понимание основного механизма является первым шагом к эффективному контролю коррозии. Ваш диагностический подход должен руководствоваться предполагаемым типом элемента.
- Если ваша основная цель — предотвращение естественной коррозии: Вероятно, вы имеете дело с электрохимическим (гальваническим) элементом. Ваше решение включает выбор совместимых материалов, их электрическую изоляцию или применение катодной защиты.
- Если вы исследуете быструю, локализованную коррозию вблизи промышленного оборудования или объектов постоянного тока: Вы почти наверняка имеете дело с электролитическим элементом. Ваш приоритет должен заключаться в обнаружении и устранении источника внешнего блуждающего тока.
В конечном итоге, знание того, происходит ли коррозия естественным образом или под воздействием внешнего фактора, определяет всю вашу стратегию предотвращения и контроля.
Сводная таблица:
| Характеристика | Электрохимический (гальванический) элемент | Электролитический элемент |
|---|---|---|
| Тип процесса | Спонтанный | Неспонтанный, принудительный |
| Преобразование энергии | Химическая → Электрическая | Электрическая → Химическая |
| Источник питания | Внутренний (химический потенциал) | Внешний источник постоянного тока |
| Полярность анода | Отрицательная | Положительная |
| Распространенный пример | Гальваническая коррозия (например, сталь/латунь) | Коррозия блуждающими токами (например, от железных дорог) |
Необходимо точно диагностировать и смягчать коррозию в вашей лаборатории или промышленном процессе?
Понимание точного типа коррозионного элемента является первым шагом к эффективному решению. Эксперты KINTEK специализируются на предоставлении точного лабораторного оборудования и расходных материалов, необходимых для анализа материалов и испытаний на коррозию. Независимо от того, исследуете ли вы гальванические реакции или эффекты блуждающих токов, у нас есть инструменты для поддержки ваших исследований и обеспечения целостности материалов.
Свяжитесь с нами сегодня через нашу контактную форму, чтобы обсудить ваши конкретные лабораторные потребности и узнать, как решения KINTEK могут улучшить ваши стратегии контроля коррозии.
Визуальное руководство
Связанные товары
- Электрохимическая ячейка для электролиза плоской коррозии
- Электрохимическая ячейка из ПТФЭ, коррозионностойкая, герметичная и негерметичная
- Электрохимическая ячейка для оценки покрытий
- Супергерметичная электрохимическая электролитическая ячейка
- Электролитическая ячейка H-типа Тройная электрохимическая ячейка
Люди также спрашивают
- Каков принцип работы электрохимической ячейки для коррозионных испытаний на плоской пластине? Руководство по контролируемому испытанию материалов
- Каковы полные постэкспериментальные процедуры для электролитической ячейки с плоской пластиной для изучения коррозии? Пошаговое руководство для получения надежных результатов
- Каковы критические меры предосторожности для обеспечения безопасности и эксплуатации электролитической ячейки с плоской пластиной для коррозии? Обеспечьте безопасное и точное электрохимическое тестирование
- Каковы конструктивные преимущества использования плоской электрохимической ячейки? Повышение точности испытаний на коррозию
- Почему для электрохимического тестирования коррозии в SBF требуется система контроля постоянной температуры? Ключ к лабораторной точности



















