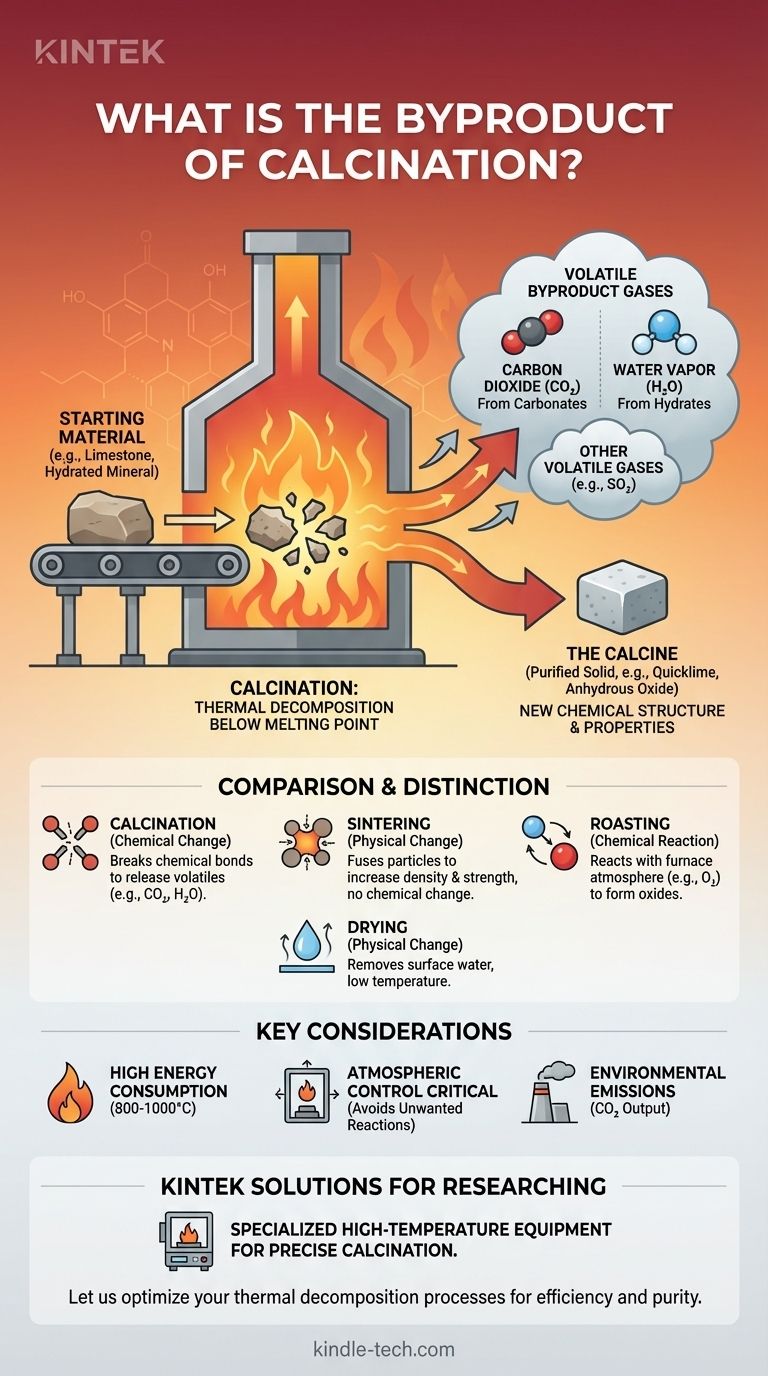
Почти во всех случаях основным побочным продуктом кальцинирования является газ. Чаще всего это углекислый газ (CO2) при нагревании карбонатов, таких как известняк, или водяной пар (H2O) при нагревании гидратированных минералов. Этот процесс представляет собой форму термического разложения, при котором интенсивный нагрев разрушает соединение до очищенного твердого вещества и летучих газов, которые удаляются.
Кальцинирование — это процесс химической трансформации, а не просто очистка. Он использует высокую температуру ниже точки плавления для разложения материала, фундаментально изменяя его химическую структуру путем удаления летучих побочных продуктов, таких как углекислый газ или водяной пар.

Что такое кальцинирование? Более глубокий взгляд
Кальцинирование — это основополагающий процесс в металлургии и материаловедении, особенно при производстве цемента, извести и при переработке некоторых руд. Понимание механизма имеет решающее значение для понимания его цели.
Основной принцип: термическое разложение
По своей сути, кальцинирование заключается в разрыве химических связей с помощью тепла. Приложенная энергия заставляет исходный материал разлагаться на два или более новых вещества.
Одно из этих веществ — желаемый твердый продукт, часто называемый «кальцинированным продуктом». Другие вещества — это газообразные побочные продукты, которые удаляются.
Объяснение распространенных побочных продуктов
Конкретный побочный продукт полностью зависит от химического состава нагреваемого материала.
- Углекислый газ (CO2): Это самый известный пример. Когда карбонат кальция (CaCO3, известняк) подвергается кальцинированию, он разлагается на оксид кальция (CaO, негашеная известь) и выделяет газ CO2. Это основная реакция в производстве цемента.
- Водяной пар (H2O): Многие минералы существуют в виде гидратов, что означает, что молекулы воды заперты в их кристаллической структуре. Кальцинирование боксита (алюминиевой руды) или гипса удаляет эту химически связанную воду в виде пара.
- Другие летучие газы: В более специфических применениях могут выделяться другие газы. Например, нагревание некоторых сульфатов может высвобождать диоксид серы (SO2), хотя этот процесс часто пересекается со смежной техникой, называемой обжигом.
Желаемый продукт: кальцинированный продукт
Твердый материал, оставшийся после удаления летучих побочных продуктов, является основной целью. Этот полученный кальцинированный продукт теперь имеет другие химические и физические свойства.
Например, негашеная известь, полученная в результате кальцинирования известняка, высокореактивна, что необходимо для производства цемента и других промышленных химикатов.
Чем кальцинирование отличается от других термических обработок
Термин «кальцинирование» часто путают с другими высокотемпературными процессами. Различие заключается в лежащей в основе химической или физической цели.
Кальцинирование против спекания
Кальцинирование изменяет химический состав материала. Оно разлагает одно соединение на другое путем удаления летучих компонентов.
Спекание, как правильно отмечено в справке, изменяет физическую форму материала. Оно использует тепло для сплавления мелких частиц вместе в единый твердый кусок, не расплавляя их, что увеличивает его прочность и плотность. Химический состав остается неизменным.
Кальцинирование против обжига
Это очень распространенный источник путаницы. Кальцинирование обычно проводится в контролируемой или инертной атмосфере для вызова разложения.
Обжиг, напротив, — это процесс, который включает химическую реакцию с атмосферой печи, в частности с кислородом. Это форма окисления, часто используемая для превращения сульфидных руд металлов в оксиды металлов.
Кальцинирование против сушки
Сушка — это низкотемпературный процесс, удаляющий физически поглощенную воду с поверхности вещества.
Кальцинирование — это высокотемпературный процесс, удаляющий химически связанную воду или другие летучие соединения из кристаллической структуры материала, требующий значительно больше энергии для разрыва этих химических связей.
Понимание подводных камней и контекста
Хотя кальцинирование является мощным, это промышленный процесс со значительными эксплуатационными соображениями, которыми необходимо управлять.
Высокое энергопотребление
Достижение и поддержание высоких температур, необходимых для разрыва химических связей (часто 800–1000°C или выше), делает кальцинирование чрезвычайно энергоемким и дорогостоящим процессом.
Контроль атмосферы имеет решающее значение
Состав газа внутри печи имеет решающее значение. Нежелательные реакции, такие как окисление из-за избытка воздуха, могут произойти, если атмосфера не будет тщательно контролироваться, что приведет к получению нечистого конечного продукта.
Экологические выбросы
Газообразные побочные продукты являются основным результатом. Кальцинирование известняка для производства цемента является одним из крупнейших промышленных источников выбросов CO2 в мире, что имеет решающее значение для управления окружающей средой и регулирования.
Выбор правильного варианта для вашей цели
Понимание кальцинирования позволяет распознать его специфическую роль в создании материалов, формирующих наш мир.
- Если ваша основная цель — производство цемента или извести: Кальцинирование — это основной процесс, используемый для разложения известняка (CaCO3) в реактивную негашеную известь (CaO) путем удаления CO2.
- Если ваша основная цель — подготовка катализатора или адсорбента: Кальцинирование используется для удаления воды и летучих прекурсоров, создавая чистый материал с высокой удельной поверхностью, готовый к использованию.
- Если ваша основная цель — упрочнение детали из керамического или металлического порошка: Вы думаете о спекании, которое уплотняет частицы для увеличения плотности, а не о кальцинировании, которое изменяет их химию.
В конечном счете, кальцинирование — это фундаментальный инструмент для химического изменения твердого материала путем использования тепла для высвобождения его летучих компонентов.
Сводная таблица:
| Материал для кальцинирования | Распространенный побочный газ | Основной твердый продукт |
|---|---|---|
| Известняк (CaCO₃) | Углекислый газ (CO₂) | Негашеная известь (CaO) |
| Гидратированные минералы (например, боксит, гипс) | Водяной пар (H₂O) | Безводный оксид |
| Некоторые сульфаты | Диоксид серы (SO₂) | Оксид металла |
Нужна точная термическая обработка ваших материалов?
Кальцинирование — критически важный этап в производстве всего: от цемента до катализаторов. KINTEK специализируется на высокотемпературном лабораторном оборудовании, включая печи, идеально подходящие для контролируемых процессов кальцинирования. Наши решения помогают вам добиться точных химических превращений, которые вам нужны, с акцентом на эффективность и чистоту.
Разрабатываете ли вы новые материалы, перерабатываете руды или готовите катализаторы, опыт KINTEK в области лабораторного оборудования может поддержать ваши исследования и контроль качества. Позвольте нам помочь вам оптимизировать ваши процессы термического разложения.
Свяжитесь с KINTEK сегодня, чтобы обсудить ваши конкретные потребности в кальцинировании и найти подходящее оборудование для вашей лаборатории.
Визуальное руководство