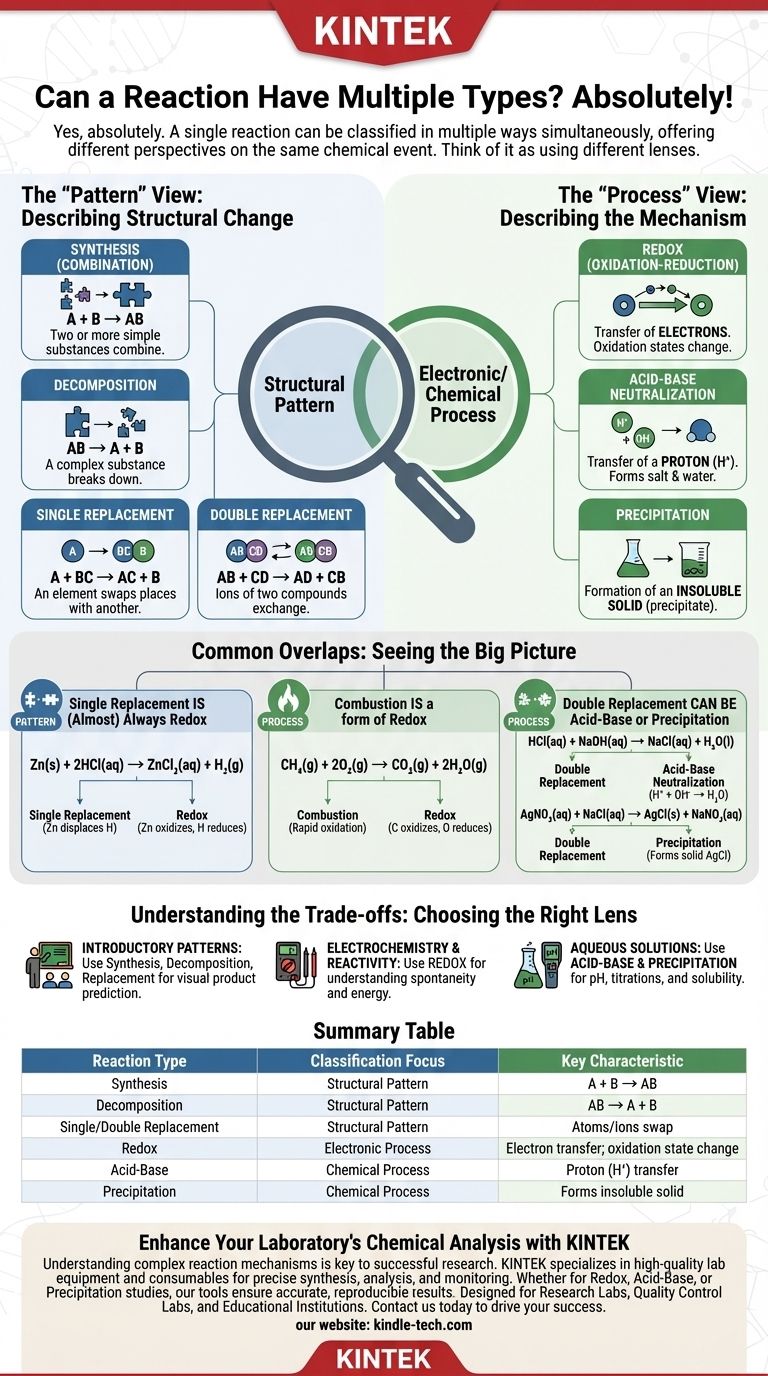
Да, безусловно. Одна химическая реакция часто может быть классифицирована как относящаяся к нескольким типам реакций одновременно. Это часто является причиной путаницы, поскольку вводный курс химии часто представляет типы реакций как взаимоисключающие категории, но более глубокое понимание показывает, что это просто разные способы анализа одного и того же химического события.
Ключ к пониманию заключается в том, что некоторые типы реакций описывают структурную закономерность того, как атомы перестраиваются (например, синтез или разложение), в то время как другие описывают лежащий в основе электронный или химический процесс (например, окислительно-восстановительные реакции или кислотно-основные реакции). Одна и та же реакция может демонстрировать как определённую закономерность, так и определённый процесс.

Почему простых ярлыков недостаточно
Способ классификации реакций зависит от того, что мы хотим о них понять. Простые категории, изучаемые в первую очередь, полезны для распознавания визуальных закономерностей, но они не всегда объясняют фундаментальное химическое изменение.
«Вид по закономерности»: описание структурных изменений
В начале изучения химии вы учитесь распознавать реакции по тому, как реагенты образуют продукты. Эти категории описывают общую «форму» превращения.
Основные типы, основанные на закономерностях:
- Синтез (или Соединение): Два или более простых вещества соединяются, образуя более сложный продукт (
A + B → AB). - Разложение: Сложное вещество распадается на более простые (
AB → A + B). - Одиночное замещение: Элемент меняется местами с другим в соединении (
A + BC → AC + B). - Двойное замещение: Ионы двух соединений обмениваются местами, образуя два новых соединения (
AB + CD → AD + CB).
Эти ярлыки отлично подходят для быстрого предсказания продуктов на основе знакомой закономерности.
«Вид по процессу»: описание механизма
Более сложные классификации описывают, как происходит превращение на молекулярном или электронном уровне. Они сосредоточены на фундаментальном процессе, движущем реакцию.
Основные типы, основанные на процессах, включают:
- Окислительно-восстановительные (ОВР): Этот тип включает перенос электронов. Степень окисления одного или нескольких элементов изменяется в ходе реакции.
- Кислотно-основная нейтрализация: Кислота и основание реагируют, обычно с переносом протона (иона H⁺) с образованием соли и воды.
- Осаждение: Две водные фазы смешиваются, и образуется нерастворимое твёрдое вещество (осадок).
Эти ярлыки необходимы для понимания основных движущих сил реакции.
Распространённые пересечения, с которыми вы столкнётесь
Понимание того, как эти категории пересекаются, — лучший способ закрепить ваше понимание. Большинство реакций, с которыми вы столкнётесь, будут иметь более одного действительного ярлыка.
Одиночное замещение (почти) всегда является окислительно-восстановительной реакцией
Рассмотрим реакцию металлического цинка с соляной кислотой:
Zn(s) + 2HCl(aq) → ZnCl₂(aq) + H₂(g)
Это классическая реакция одиночного замещения, потому что цинк вытесняет водород. Однако это также окислительно-восстановительная реакция, потому что степени окисления изменяются: цинк окисляется (от 0 до +2), а водород восстанавливается (от +1 до 0).
Горение — это форма окислительно-восстановительной реакции
Хорошим примером является горение метана:
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
Хотя мы называем это горением, это также фундаментально окислительно-восстановительная реакция. Углерод окисляется (от -4 до +4), а кислород восстанавливается (от 0 до -2).
Двойное замещение может быть кислотно-основной реакцией или реакцией осаждения
Рассмотрим нейтрализацию соляной кислоты гидроксидом натрия:
HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)
Это реакция двойного замещения; Na⁺ и H⁺ меняются местами. Что более важно, это яркий пример кислотно-основной нейтрализации.
Аналогично, смешивание нитрата серебра и хлорида натрия:
AgNO₃(aq) + NaCl(aq) → AgCl(s) + NaNO₃(aq)
Это соответствует схеме двойного замещения, но её наиболее примечательной особенностью является образование твёрдого вещества, что делает её реакцией осаждения.
Понимание компромиссов: цель классификации
Выбор ярлыка не означает поиск единственно «правильного» ответа. Речь идёт об использовании наиболее точного и полезного ярлыка для вашей конкретной цели.
Ограничения простых закономерностей
Классификация реакции как «одиночного замещения» говорит о том, что произошло с атомами, но не объясняет, почему это произошло. Она не объясняет, почему цинк реагирует с HCl, а медь нет.
Сила механистических ярлыков
Идентификация той же реакции как «окислительно-восстановительной» даёт гораздо более глубокое понимание. Она позволяет использовать такие понятия, как ряд активности или стандартные электродные потенциалы, для предсказания, произойдёт ли реакция спонтанно, и для количественной оценки задействованной энергии. Ярлык «окислительно-восстановительная» объясняет «почему».
Правильный выбор для вашей цели
Используйте ту классификацию, которая наилучшим образом служит вашей цели. Цель состоит не в том, чтобы найти единственный, исключительный ярлык, а в том, чтобы применить наиболее релевантный.
- Если ваша основная цель — распознавание основных закономерностей на вводном курсе: Придерживайтесь синтеза, разложения и одиночного/двойного замещения для визуального предсказания продуктов.
- Если ваша основная цель — электрохимия или предсказание реакционной способности: Классификация окислительно-восстановительных реакций является наиболее важным подходом.
- Если ваша основная цель — работа с водными растворами, pH и титрованием: Классификация реакций как кислотно-основных или осаждения будет наиболее полезным подходом.
В конечном итоге, использование правильного ярлыка зависит от конкретного вопроса, на который вы пытаетесь ответить относительно химического превращения.
Сводная таблица:
| Тип реакции | Фокус классификации | Ключевая характеристика |
|---|---|---|
| Синтез | Структурная закономерность | Два или более реагента объединяются в один продукт (A + B → AB) |
| Разложение | Структурная закономерность | Одно соединение распадается на более простые вещества (AB → A + B) |
| Одиночное/Двойное замещение | Структурная закономерность | Атомы или ионы меняются местами между соединениями |
| Окислительно-восстановительная | Электронный процесс | Включает перенос электронов; изменяются степени окисления |
| Кислотно-основная | Химический процесс | Включает перенос протона (H⁺) |
| Осаждение | Химический процесс | Образование нерастворимого твёрдого вещества из водных растворов |
Повысьте эффективность химического анализа вашей лаборатории с KINTEK
Понимание сложных механизмов реакций является ключом к успешным исследованиям и разработкам. В KINTEK мы специализируемся на предоставлении высококачественного лабораторного оборудования и расходных материалов, которые поддерживают точный химический синтез, анализ и мониторинг процессов. Независимо от того, работаете ли вы над окислительно-восстановительными реакциями, кислотно-основным титрованием или исследованиями осаждения, наши надёжные инструменты помогут вам достичь точных и воспроизводимых результатов.
Наши продукты разработаны для:
- Исследовательских лабораторий, требующих точного контроля температуры для реакций синтеза и разложения.
- Лабораторий контроля качества, нуждающихся в стабильном оборудовании для кислотно-основного анализа и анализа осаждения.
- Образовательных учреждений, ищущих долговечное и простое в использовании оборудование для преподавания фундаментальных и продвинутых типов реакций.
Пусть KINTEK станет вашим надёжным партнёром в развитии возможностей вашей лаборатории. Свяжитесь с нами сегодня, чтобы обсудить ваши конкретные потребности и узнать, как наши решения могут способствовать вашему успеху.
Визуальное руководство