Иллюзия простоты
В лаборатории мы часто зацикливаемся на сложности электролита. Мы измеряем концентрации до микрограмма. Мы одержимы температурными градиентами. Мы относимся к химическому раствору как к деликатному рецепту, требующему прикосновения шеф-повара.
Однако мы часто упускаем из виду «водопровод» эксперимента: провода.
Подключение электролитической ячейки кажется тривиальным. Красный провод сюда, черный провод туда. Это похоже на подключение тостера — действительно ли имеет значение, в какую сторону?
В электролизе это имеет значение больше, чем что-либо еще.
Полярность электродов — это не просто деталь соединения. Это центр управления вашим экспериментом. Это разница между созданием шедевра и растворением вашего оборудования.
Электронный насос
Чтобы понять полярность, вы должны перестать думать об источнике питания как о батарее и начать думать о нем как о насосе.
В отличие от гальванической ячейки, где химия создает электричество, электролитическая ячейка использует электричество, чтобы заставить химию происходить против ее воли. Реакция несамопроизвольна. Ей нужен толчок.
Источник питания обеспечивает этот толчок, но строго в одном направлении:
- Он вытягивает электроны с одной стороны.
- Он толкает электроны к другой.
Этот поток определяет идентичность ваших электродов. Метки «Анод» и «Катод» — это не географические места в вашей колбе; это функциональные роли, определяемые исключительно этим потоком.
Анод: Великий удалитель
Подключенный к положительному (+) клемме, анод — это место, где источник питания вырывает электроны из химических частиц.
Это место окисления. Молекулы рядом с этой поверхностью теряют электроны. Они «раздеваются».
Катод: Великий даритель
Подключенный к отрицательному (-) клемме, катод — это место, где источник питания навязывает избыток электронов на поверхность.
Это место восстановления. Молекулы рядом с этой поверхностью получают электроны. Они «наращиваются».
Цена ошибки
Что произойдет, если вы поменяете провода местами?
Во многих сферах жизни обратное подключение просто означает, что устройство не включается. В электролизе последствия гораздо более активны — и часто разрушительны.
Когда вы меняете полярность, вы не останавливаете реакцию. Вы инвертируете вселенную вашей колбы.
1. Вы создаете не ту реальность
Если вы намеревались получить кислород, но перепутали клеммы, вы можете получить водород. Химическая логика полностью инвертирована. Вы получаете не «отсутствие результата», а «анти-результат».
2. Вы растворяете свои активы
Представьте, что вы покрываете старинный ключ медью методом гальваностегии. Вы хотите, чтобы ионы меди осадились на ключ.
Если вы измените полярность, ключ станет анодом (местом окисления). Вместо того чтобы получить блестящее покрытие медью, сам ключ начнет растворяться в растворе. Вы не сохраняете объект; вы активно его уничтожаете.
3. Вы загрязняете среду
Принудительное окисление на электроде, не предназначенном для этого, приводит к быстрой коррозии. Это не только разрушает электрод; это насыщает ваш тщательно подготовленный электролит загрязнителями, делая весь эксперимент недействительным.
Хореография атомов
Успешный электролиз требует от вас быть архитектором атомного движения. Вы должны решить, куда пойдут электроны, прежде чем нажать на выключатель.
Используйте эту логику для назначения полярности:
-
Цель: Гальваностегия
- Настройка: Объект, который нужно покрыть, должен быть катодом (-).
- Физика: Положительные ионы металла должны получить электроны и превратиться в твердый металл на поверхности объекта.
-
Цель: Производство газа (например, кислорода)
- Настройка: Место сбора должно быть анодом (+).
- Физика: Молекулы воды должны терять электроны (окисляться), чтобы выделить газообразный кислород.
-
Цель: Рафинирование металлов
- Настройка: Нечистый металл должен быть анодом (+).
- Физика: Сырой металл должен раствориться (окислиться) в растворе, чтобы его можно было осадить в чистом виде в другом месте.
Сводка управления
Вот шпаргалка для управления вашей химической судьбой:
| Электрод | Подключение | Реакция | Физический механизм |
|---|---|---|---|
| Анод | Положительный (+) | Окисление | Электроны отбираются; материалы растворяются или выделяют газ. |
| Катод | Отрицательный (-) | Восстановление | Электроны добавляются; материалы покрываются или очищаются. |
Точность исполнения
В электролизе есть определенная романтика. Вы проникаете в молекулярный мир и заставляете атомы маршировать в выбранном вами направлении.
Но этот контроль зависит от целостности вашей установки. Даже лучшее теоретическое понимание терпит неудачу, если оборудование ненадежно или соединения плохие.
В KINTEK мы понимаем, что грань между прорывом и неудачным экспериментом часто так же тонка, как соединение проводов. Мы специализируемся на высокоточном лабораторном оборудовании и расходных материалах, разработанных для обеспечения абсолютного контроля над вашими электрохимическими процессами.
Независимо от того, рафинируете ли вы драгоценные металлы или проводите чувствительные исследования, наши инструменты гарантируют, что когда вы командуете электронам течь, они идут именно туда, куда должны.
Не позволяйте простому изменению полярности стоить вам времени и образцов. Свяжитесь с нашими экспертами
Визуальное руководство
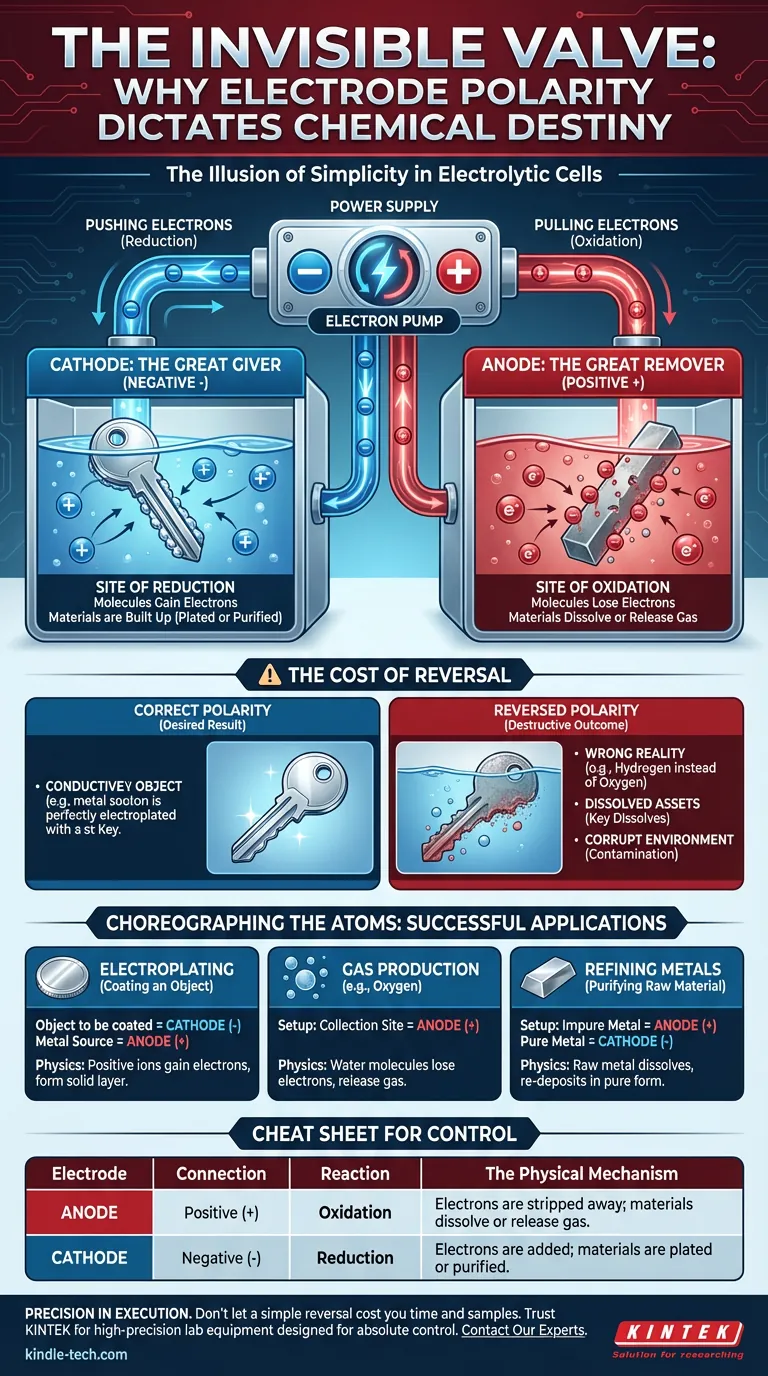
Связанные товары
- Электрохимическая ячейка из ПТФЭ, коррозионностойкая, герметичная и негерметичная
- Супергерметичная электрохимическая электролитическая ячейка
- Электрохимическая ячейка с пятью портами
- Электролитическая ячейка H-типа Тройная электрохимическая ячейка
- Электрохимическая ячейка с газодиффузионным электролизом и ячейка для реакции с протоком жидкости
Связанные статьи
- Архитектура определенности: освоение контроля в многофункциональных электролитических ячейках
- Электролитические батареи Решение для растущих потребностей в энергии
- Якорь истины: почему физическая стабильность определяет электрохимический успех
- Тихая геометрия напряжения: Соблюдение пределов электролиза
- Искусство сопротивления: почему вашей электролитической ячейке нужно пространство для дыхания




















