Введение в измерение стационарных состояний
Процессы электродных реакций
Электродные реакции - это многогранные процессы, которые включают в себя как нефарадеевские, так и фарадеевские механизмы. Эти механизмы находят свое отражение в соответствующих плотностях тока: нефарадеевских и фарадеевских плотностях тока.
-
Нефарадеевские процессы: Эти процессы не связаны с переносом заряда через границу раздела электрод-электролит. Вместо этого они обычно связаны с явлениями адсорбции или десорбции, поверхностной диффузией или другими взаимодействиями, связанными с поверхностью, которые не способствуют чистому переносу заряда. Нефарадеевская плотность тока свидетельствует об этих поверхностно-связанных процессах, давая представление о состоянии и динамике поверхности электрода.
-
Фарадеевские процессы: Напротив, процессы Фарадея включают в себя фактический перенос заряда через границу раздела электрод-электролит, что приводит к химическим превращениям, таким как реакции окисления или восстановления. Плотность тока Фарадея является прямой мерой этих процессов переноса заряда, предоставляя критическую информацию о кинетике и термодинамике электродных реакций.

Понимание взаимосвязи между этими двумя типами процессов имеет решающее значение для точной интерпретации измерений стационарного состояния в электрохимии. Баланс между нефарадеевскими и фарадеевскими плотностями тока дает полное представление о поведении электрода в различных условиях, помогая оптимизировать электрохимические системы для различных применений - от накопления энергии до катализа.
Измерения в стационарном состоянии и переходные процессы
Измерения в стационарном состоянии в электрохимии характеризуются стабилизацией плотности тока Фарадея, что происходит, когда электродные реакции достигают состояния равновесия, при котором чистый поток носителей заряда остается постоянным во времени. Это резко отличается от переходных измерений, где плотность тока Фарадея зависит от времени, отражая динамическую природу электродных процессов при их переходе из одного состояния в другое.
В устойчивом состоянии скорость прямой и обратной реакций на поверхности электрода уравновешена, что приводит к стабильной плотности тока, которая не колеблется со временем. Такая стабильность позволяет проводить точные измерения и анализ кинетики электрода и механизмов реакции. С другой стороны, переходные измерения фиксируют начальные стадии электродных реакций, позволяя понять зависящее от времени поведение плотности тока при переходе системы из одного устойчивого состояния в другое.
Различие между измерениями в установившемся состоянии и переходными процессами имеет решающее значение для понимания механизмов, лежащих в основе электродных реакций. Измерения в установившемся состоянии особенно полезны для изучения долгосрочного поведения и стабильности электрохимических систем, в то время как измерения в переходном режиме позволяют получить детальное представление о реакции системы на изменение экспериментальных условий, таких как возмущения потенциала или тока.
Подводя итог, можно сказать, что если измерения в установившемся состоянии позволяют получить моментальный снимок стабильных условий в электрохимической системе, то измерения в переходном режиме дают динамическое представление о том, как эти условия устанавливаются и изменяются с течением времени. Оба метода необходимы для всестороннего понимания электрохимических процессов, каждый из них вносит свой уникальный вклад в поведение электродных реакций.
Характеристики стационарного состояния
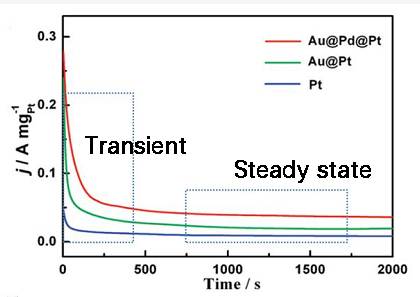
Стационарное состояние в сравнении с равновесным состоянием
В области электрохимии понимание различий между устойчивым и равновесным состоянием имеет решающее значение для точных измерений и анализа. Устойчивое состояние характеризуется наличием чистого тока, что указывает на продолжающиеся электрохимические процессы, которые поддерживают стабильное состояние в течение долгого времени. Это резко контрастирует с равновесного состояния в котором нет чистого тока, что означает равновесие между прямой и обратной реакциями.
Чтобы прояснить это различие, рассмотрим следующие моменты:
-
Наличие чистого тока: В устойчивом состоянии чистый ток не равен нулю, что отражает непрерывное протекание электрохимических реакций. Это важно для процессов, в которых система должна поддерживать постоянный выход или состояние, например, в батареях или топливных элементах.
-
Отсутствие чистого тока в равновесии: Напротив, равновесное состояние характеризуется отсутствием чистого тока. Здесь скорости прямой и обратной реакций равны, что не приводит к общим изменениям в системе. Это похоже на химическую систему в состоянии покоя, где концентрации реактантов и продуктов остаются постоянными.
| Аспект | Стационарное состояние | Равновесное состояние |
|---|---|---|
| Чистый ток | Присутствует | Отсутствует |
| Динамика реакций | Непрерывные, стабильные реакции | Сбалансированные прямые и обратные реакции |
| Стабильность системы | Стабильна в течение определенного периода | Постоянно стабильная, без чистых изменений |
Это различие имеет ключевое значение для различных электрохимических приложений, поскольку помогает исследователям и инженерам определить условия работы, которые наилучшим образом соответствуют их потребностям, будь то поддержание непрерывного потока тока или достижение сбалансированной, стабильной системы.
Относительная природа устойчивого состояния
Устойчивое состояние - это не абсолютное понятие, а скорее относительное. В электрохимических системах состояние считается устойчивым, если условия, такие как плотность тока, потенциал и профиль концентрации, остаются стабильными в течение определенного периода времени. Эта стабильность имеет решающее значение для точных измерений и надежного анализа данных.
Относительная природа устойчивого состояния подразумевает, что то, что считается устойчивым, может меняться в зависимости от контекста и конкретных требований эксперимента. Например, в некоторых экспериментах устойчивое состояние может быть достигнуто в течение нескольких минут, в то время как в других это может занять часы или даже дни. Длительность стабильного состояния часто определяется чувствительностью измерительных приборов и скоростью, с которой система может достичь равновесия.
Кроме того, понятие устойчивого состояния часто сравнивают с переходными состояниями, когда условия меняются с течением времени. В отличие от переходных измерений, измерения в устойчивом состоянии дают моментальный снимок системы, когда она установилась в предсказуемом режиме. Эта предсказуемость важна для понимания электрохимических процессов, лежащих в их основе, и для проведения значимых сравнений между различными экспериментальными условиями.
В целом, устойчивое состояние - это динамическое равновесие, при котором условия стабильны, но не обязательно постоянны. Это относительное понятие, которое зависит от конкретных условий и продолжительности, в течение которой наблюдается стабильность. Это понимание является основополагающим для точной интерпретации измерений устойчивого состояния в электрохимии.
Методы измерения стационарного состояния
Метод постоянного потенциала
Метод постоянного потенциала является ключевым методом в электрохимических исследованиях, особенно в измерениях установившегося состояния. В этом методе используется измеритель постоянного потенциала для тщательного контроля потенциала, обеспечивая статическое или динамическое изменение потенциала. Поддерживая постоянный потенциал, исследователи могут наблюдать и анализировать поведение электродных реакций в контролируемых условиях.
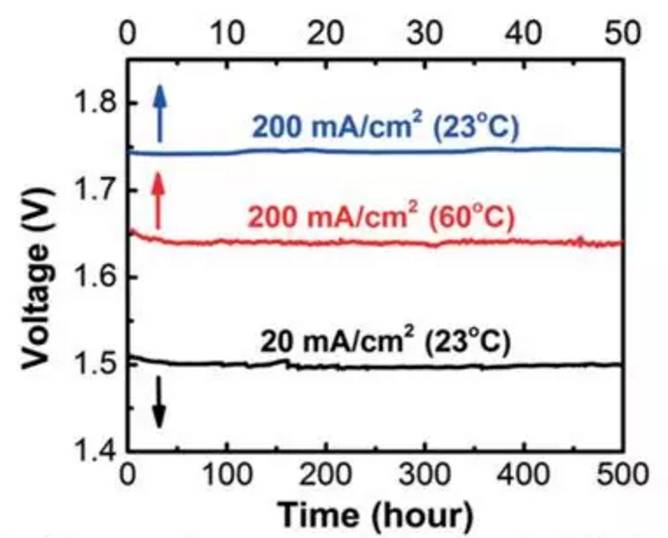
При использовании статического потенциала потенциал остается неизменным на протяжении всего эксперимента, что позволяет детально наблюдать за реакцией системы на фиксированное условие. С другой стороны, при использовании динамического потенциала потенциал изменяется с течением времени, что позволяет понять, как система адаптируется к изменяющимся условиям. Такой двойной подход позволяет всесторонне понять как стабильные, так и развивающиеся электрохимические процессы.
Метод постоянного потенциала помогает достичь устойчивого состояния, при котором плотность тока Фарадея стабилизируется. Это очень важно для точного измерения и интерпретации кинетики электродов, так как устраняет осложнения, возникающие из-за переходных эффектов. Контролируя потенциал, исследователи могут систематически изучать взаимосвязь между потенциалом и плотностью тока, что облегчает определение критических параметров и характеристик реакции.
Таким образом, метод постоянного потенциала представляет собой надежную основу для контроля и анализа электрохимических процессов как в статических, так и в динамических условиях. Способность стабилизировать потенциал и плотность тока делает его незаменимым инструментом при изучении электродных реакций и их кинетики.
Метод постоянного тока
Метод постоянного тока является ключевым в электрохимических исследованиях, особенно в области измерений в установившемся режиме. Этот метод предполагает тщательный контроль внешнего тока для установления стабильных значений потенциала при различной плотности тока. Поддерживая постоянный ток, исследователи могут наблюдать за тем, как реагирует потенциал электродной системы, что позволяет получить ценные сведения об электрохимическом поведении системы.
Одним из главных преимуществ метода постоянного тока является его способность стабилизировать электрохимическую систему, что позволяет проводить точные измерения изменения потенциала. Такая стабильность очень важна для понимания кинетики электродных реакций, поскольку она устраняет переходные эффекты, характерные для измерений, зависящих от времени. Метод особенно полезен в сценариях, где плотность тока является критическим параметром, например, при изучении коррозии, работы аккумуляторов и процессов электроосаждения.
В практических приложениях метод постоянного тока часто используется в сочетании с другими методами, такими как метод вращающегося дискового электрода (RDE) и метод поляризационной кривой в стационарном состоянии. Эти комбинированные подходы позволяют провести всесторонний анализ электродной кинетики, обеспечивая более глубокое понимание механизмов реакции и кинетических параметров. Например, систематически изменяя плотность тока и измеряя соответствующий потенциал, исследователи могут построить поляризационные кривые, которые выявляют критические точки, такие как потенциал коррозии и предельная плотность тока.
Кроме того, метод постоянного тока играет важную роль в разработке электрохимических датчиков и устройств. Точно контролируя ток, можно оптимизировать работу этих устройств, обеспечивая надежность и точность измерений. Этот метод также важен для калибровки электрохимических приборов, поскольку он обеспечивает стандартизированный подход к измерению потенциала в контролируемых условиях.
Таким образом, метод постоянного тока играет важную роль в области электрохимии, предлагая надежный подход к изучению электродных реакций и стабильности системы. Его способность обеспечивать стабильные и воспроизводимые измерения делает его незаменимым инструментом как для фундаментальных исследований, так и для практических применений.
Поляризационная кривая стационарного состояния
Поляризационная кривая в стационарном состоянии является ключевым методом в области электрохимии, служащим важнейшим инструментом для разгадки сложной динамики электродных реакций. Этот метод помогает не только выяснить фундаментальные характеристики этих реакций, но и извлечь важнейшие кинетические параметры, определяющие их поведение. Систематически отображая взаимосвязь между потенциалом электрода и плотностью тока, поляризационная кривая дает полное представление о том, как различные факторы влияют на общую кинетику реакции.
Чтобы глубже понять значение поляризационной кривой в стационарном состоянии, необходимо понять ее роль в более широком контексте электрохимических исследований. В отличие от переходных измерений, которые сосредоточены на изменениях, зависящих от времени, измерения в установившемся состоянии направлены на стабилизацию плотности тока Фарадея, обеспечивая тем самым более стабильную и надежную основу для анализа. Эта стабильность имеет решающее значение для точного определения кинетических параметров, таких как константы скорости реакции и коэффициенты переноса, которые имеют ключевое значение для разработки эффективных электрохимических систем.
Кроме того, поляризационная кривая в стационарном состоянии особенно ценна для различения различных путей и механизмов реакции. Анализируя кривую, исследователи могут определить наличие нескольких стадий реакции, адсорбционных процессов и других межфазных явлений, которые в противном случае могли бы остаться незамеченными. Эти возможности еще более расширяются в сочетании с такими методами, как вращающийся дисковый электрод (RDE), который помогает быстрее свести электродные реакции к устойчивому состоянию, тем самым минимизируя влияние переходных эффектов.
По сути, поляризационная кривая устойчивого состояния - это не просто диагностический инструмент, а краеугольный камень в систематическом изучении кинетики электродов. Ее способность давать детальное представление о механизмах реакции и кинетических параметрах делает ее незаменимым методом как для фундаментальных исследований, так и для практического применения в электрохимии.
Вращающийся дисковый электрод (RDE)
Вращающийся дисковый электрод (ВДЭ) - это специализированный гидродинамический рабочий электрод, используемый в трехэлектродной системе и предназначенный в первую очередь для сведения электродных реакций к устойчивому состоянию. Эта техника особенно эффективна для устранения эффекта двойного слоя - области ионного заряда у поверхности электрода, которая может мешать точным измерениям. Контролируя поток электролита, RDE обеспечивает последовательный и предсказуемый массовый перенос реактивов к поверхности электрода, что способствует проведению точных электрохимических исследований.

В практических приложениях RDE используется в различных электрохимических экспериментах, включая изучение коррозии, исследование топливных элементов и разработку катализаторов. Вращение электрода во время экспериментов создает постоянный поток аналита к электроду, что очень важно для поддержания стабильных условий. Такая установка особенно удобна в сценариях, где необходим определенный массоперенос к электроду образца, например, при оценке катализатора.
Структура RDE включает в себя проводящий диск, встроенный в инертный, непроводящий полимер или смолу, который затем прикреплен к электродвигателю с возможностью точного контроля скорости вращения электрода. Диск, обычно изготавливаемый из благородных металлов, таких как платина или золото, или стеклоуглерода, может быть изготовлен из любого проводящего материала в соответствии с конкретными экспериментальными требованиями. Такая гибкость в выборе материала в сочетании с точным контролем над вращением делает RDE универсальным инструментом в области электрохимии.
В аналитической химии RDE используется в трехэлектродных системах для гидродинамической вольтамперометрии. Его вращающийся механизм вызывает приток аналита к электроду, что делает его идеальным для изучения механизмов реакций, связанных с окислительно-восстановительной химией и другими химическими явлениями. Для более сложных исследований вращающийся электрод с кольцом и диском может быть адаптирован, при этом кольцо остается неактивным и функционирует исключительно как RDE. Такая адаптация еще больше расширяет возможности использования RDE в различных электрохимических приложениях.
Связанные товары
- Лабораторная электрохимическая рабочая станция Потенциостат для лабораторного использования
- Опорный корпус образца для электрохимических испытаний
- Электрохимическая ячейка с пятью портами
- Электрохимическая ячейка для электролиза плоской коррозии
- Электрохимическая ячейка для оценки покрытий
Связанные статьи
- Unlocking Purity: Полное руководство по портативным анализаторам драгоценных металлов
- Основное лабораторное реакционное оборудование
- Как выбрать правильный электрохимический электрод
- Понимание электроосаждения с помощью электрохимических электродов
- Инновации в технологии электрохимических электродов
















